ФИЗИКО-ХИМИЧЕСКОЕ СОПОСТАВЛЕНИЕ РЕАГЕНТНЫХ МЕТОДОВ ОЧИСТКИ СТОЧНЫХ ВОД ОТ ИОНОВ ТЯЖЕЛЫХ МЕТАЛЛОВ
Принцип рационального природопользования предусматривает минимизацию потрeбления свежей воды на технологические нужды за счет высокоэффективной очистки сточных вод и организации оборотного водоснабжения.
Машиностроительные и металлообpaбатывающие производства являются значительными потребителями водных ресурсов, забирающими из водных источников около 12% свежей воды от общего расхода промышленностью страны. Около половины этого количества расходуется на нужды гальванического производства. Применяемые методы очистки сточных вод от ионов тяжелых металлов (Cd2+, Сo2+, Сu2+, Mn2+, Zn2+, Pb2+, Ni2+, Сr3+) свидетельствуют о серьезном загрязнении природной среды и расточительном отношении к ресурсам.
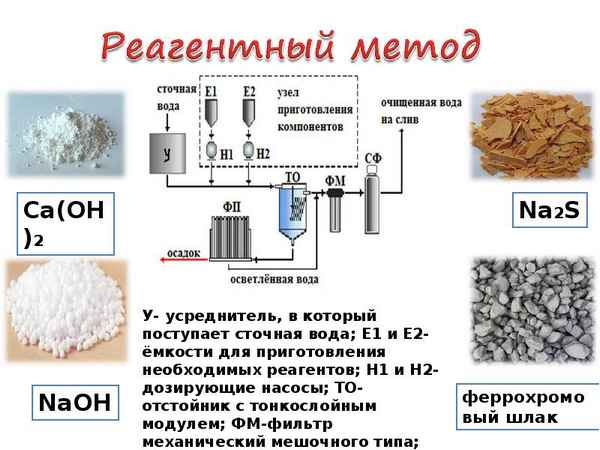
Наиболее распространен реагентный метод, основанный на переводе ионов тяжелых металлов в малорастворимые гидроксиды. В последние годы разработан и получает распространение сульфидный метод, предусматривающий осаждение тяжелых металлов в форме сульфидов. В патентной литературе имеются сведения об эффективности осаждения тяжелых металлов в виде фосфатов.
Целью настоящей работы является сравнение эффективности гидроксидного, сульфидного и фосфатного метода очисти сточных вод от ионов тяжелых металлов.
Остаточное содержание ионов тяжелых металлов в сточных водах после осаждения их в форме гидроксидов, сульфидов и фосфатов равно растворимости осадка над раствором. Расчет растворимости гидроксидов проведен с учетом образования гидроксокомплексов (на примере двухзарядных катионов)
Для фосфатов и сульфидов учитывались реакции гидролиза анионов:
Константы равновесия соответствующих реакций и произведения растворимости (ПР) взяты по литературным данным.
Растворимость гидроксидов металлов (S) описывается уравнением:
где К1, К2, ... - ступенчатые константы образования гидроксокомплексов.
Для растворимости фосфатов получено выражение
В этом выражении К1, К2, К3 - ступенчатые константы диссоциации фосфорной кислоты.
Растворимость сульфидов описывается уравнением:
,
где К1, К2 - ступенчатые константы диссоциации сероводорода.
Аналогичным образом получены соответствующие уравнения для растворимости солей трехзарядных катионов (Fe3+ , Сr3+).
Полученные значения S (моль/л) пересчитывались на содержание ионов данного металла в мг/л. Степень очистки сточных вод (СО) хаpaктеризовали степенью достижения требований ПДК для водоемов хозяйственно-питьевого водопользования (СОхпв) и рыбохозяйственного назначения (СОрхн) в соответствии с формулой
.
При значениях СО≥100% очистка сточных вод до требований ПДК достигается, при СО<100% - нет.
Результаты расчетов представлены в табл.
Как следует из полученных данных, сульфидный метод обеспечивает очистку сточных вод в интервале рН, допустимого для сброса сточных вод во все водоемы (6,5-8,5) пpaктически для всех металлов, кроме марганца.
Фосфатный метод обеспечивает аналогичную очистку сточных вод при рН≤8,5 для Pb2+, Fe3+ и Cr3+, а в более щелочных средах (при рН≤11) для Co2+, Cu2+ и Mn2+, причем только для водоемов хозяйственно-питьевого водопользования. При рН >11 дополнительно могут быть осаждены также ионы Ni2+, Zn2+ и Fe2+.
Таблица. Сопоставительный анализ реагентных методов
|
Ион металла |
Гидроксидный метод |
Фосфатный метод |
Сульфидный метод |
||||||
|
Интервал рН |
СОхпв, % |
СОрхн, % |
Интервал рН |
СОхпв, % |
СОрхн, % |
Интервал рН |
СОхпв, % |
СОрхн, % |
|
|
Cd2+ |
11-13 |
<1 |
<1 |
>11 |
1 |
5 |
6,5-8,5 |
>100 |
>100 |
|
Co2+ |
10-12 |
67 |
7 |
10-11 |
>100 |
14 |
6,5-8,5 |
>100 |
>100 |
|
Cu2+ |
8-12 |
>100 |
<1 |
7,5-8,5 |
>100 |
<1 |
6,5-8,5 |
>100 |
>100 |
|
Mn2+ |
11,2-12,5 |
100 |
10 |
9-10,5 |
>100 |
12 |
>11 |
100 |
<1 |
|
Ni2+ |
9,7-10,7 |
<1 |
<1 |
>11 |
100 |
10 |
7,0-8,5 |
>100 |
>100 |
|
Pb2+ |
10,5-11,5 |
<1 |
2 |
8-10 |
100 |
>100 |
6,5-8,5 |
>100 |
>100 |
|
Zn2+ |
9-11 |
33 |
<1 |
>11 |
100 |
1 |
6,5-8,5 |
>100 |
>100 |
|
Fe2+ |
10,5-11 |
>100 |
>100 |
>11 |
100 |
30 |
7,5-8,5 |
>100 |
>100 |
|
Fe3+ |
5,5-8,5 |
>100 |
>100 |
6,5-11 |
>>100 |
>>100 |
6,5-8,5 |
>100 |
>100 |
|
Cr3+ |
8,5-10 |
>100 |
>100 |
7,5-11 |
>100 |
>100 |
Переход в Cr(OH)3 |
||
Гидроксидный метод эффективен для удаления только ионов Fe3+, однако в более щелочных средах могут быть удалены Cu2+ (для водоемов хозяйственно-питьевого водопользования), Fe2+ и Cr3+.
Таким образом, наиболее эффективным методом является сульфидный; фосфатный метод может быть использован только для определенного состава сточных вод; гидроксидный метод, получивший наибольшее распространение, не обеспечивает необходимой степени очистки сточных вод.
 Статья в формате PDF
196 KB...
Статья в формате PDF
196 KB...
23 05 2026 7:56:41
 В работе рассмотрена очистка природных вод от ионов жесткости с помощью сорбентов на основе выщелоченных базальтовых волокон, модифицированных бентонитовой глиной. Определены статические и динамические параметры очистки.
...
В работе рассмотрена очистка природных вод от ионов жесткости с помощью сорбентов на основе выщелоченных базальтовых волокон, модифицированных бентонитовой глиной. Определены статические и динамические параметры очистки.
...
20 05 2026 9:19:43
 Статья в формате PDF
121 KB...
Статья в формате PDF
121 KB...
18 05 2026 20:38:55
 Статья в формате PDF
119 KB...
Статья в формате PDF
119 KB...
15 05 2026 14:34:46
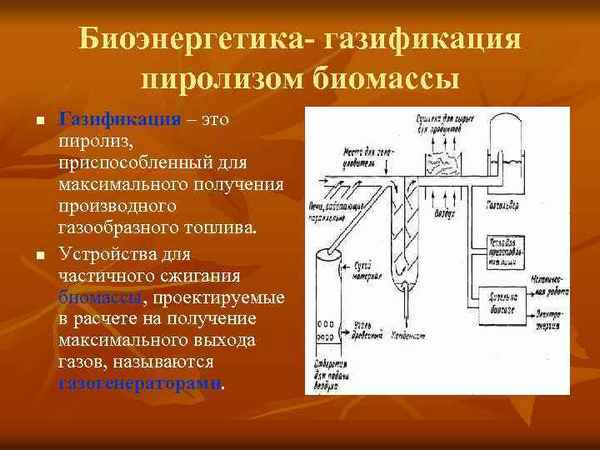 В последние годы для сжигания как традиционных топлив, так и биомасс различного происхождения широко применяются газификационные технологии. Газификация чаще всего производится в кипящем слое при недостатке окислителя. Конструкции установок по газификации различных топлив отличаются, но не принципиально. Также близкими оказываются и параметры генераторного газа. Необходимо развитие установок и технологий по совместной переработке различных топлив.
...
В последние годы для сжигания как традиционных топлив, так и биомасс различного происхождения широко применяются газификационные технологии. Газификация чаще всего производится в кипящем слое при недостатке окислителя. Конструкции установок по газификации различных топлив отличаются, но не принципиально. Также близкими оказываются и параметры генераторного газа. Необходимо развитие установок и технологий по совместной переработке различных топлив.
...
14 05 2026 18:29:53
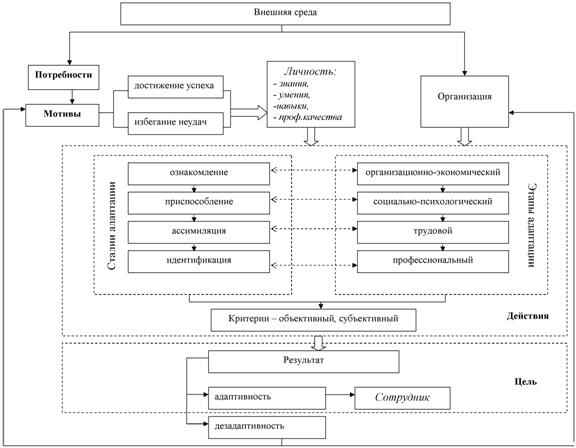 В статье рассматриваются социальный успех, успешность, успешная деятельность, как основные категории самореализации и профессионального роста. Анализируется проблема влияния современного общества на мотивационную сферу личности в деятельности. Представлена модель влияния мотивов «достижения успеха» на трудовую адаптацию личности.
...
В статье рассматриваются социальный успех, успешность, успешная деятельность, как основные категории самореализации и профессионального роста. Анализируется проблема влияния современного общества на мотивационную сферу личности в деятельности. Представлена модель влияния мотивов «достижения успеха» на трудовую адаптацию личности.
...
12 05 2026 10:28:36
11 05 2026 9:49:36
 Статья в формате PDF
114 KB...
Статья в формате PDF
114 KB...
10 05 2026 6:39:43
 Статья в формате PDF
139 KB...
Статья в формате PDF
139 KB...
09 05 2026 11:37:12
 Статья в формате PDF
115 KB...
Статья в формате PDF
115 KB...
08 05 2026 3:51:34
 Статья в формате PDF
123 KB...
Статья в формате PDF
123 KB...
07 05 2026 10:18:39
 Статья в формате PDF
124 KB...
Статья в формате PDF
124 KB...
06 05 2026 16:10:11
Статья в формате PDF 119 KB...
05 05 2026 10:34:54
 Статья в формате PDF
294 KB...
Статья в формате PDF
294 KB...
04 05 2026 20:39:44
 Статья в формате PDF
131 KB...
Статья в формате PDF
131 KB...
03 05 2026 10:22:15
 Статья в формате PDF
107 KB...
Статья в формате PDF
107 KB...
02 05 2026 13:24:17
 Статья в формате PDF
107 KB...
Статья в формате PDF
107 KB...
01 05 2026 19:23:59
30 04 2026 16:14:38
 Статья в формате PDF
258 KB...
Статья в формате PDF
258 KB...
29 04 2026 12:35:55
 Статья в формате PDF
123 KB...
Статья в формате PDF
123 KB...
28 04 2026 17:38:11
 Статья в формате PDF
251 KB...
Статья в формате PDF
251 KB...
27 04 2026 8:12:20
25 04 2026 3:36:12
 Статья в формате PDF
354 KB...
Статья в формате PDF
354 KB...
24 04 2026 14:48:17
 Статья в формате PDF
245 KB...
Статья в формате PDF
245 KB...
23 04 2026 23:13:54
 Статья в формате PDF
110 KB...
Статья в формате PDF
110 KB...
21 04 2026 21:41:20
 Статья в формате PDF
102 KB...
Статья в формате PDF
102 KB...
20 04 2026 7:45:17
 Статья в формате PDF
112 KB...
Статья в формате PDF
112 KB...
18 04 2026 0:52:33
 Существующие методы атомной эмиссионной спектроскопии для исследования состава металлов и сплавов используются во всех отраслях машиностроения. По мнению авторов, современные методы уже не обеспечивают необходимых точностей измерений.
В данной работе авторами проведены исследования влияния внешних факторов на точность измерений прибора атомно-эмиссионной спектроскопии.
...
Существующие методы атомной эмиссионной спектроскопии для исследования состава металлов и сплавов используются во всех отраслях машиностроения. По мнению авторов, современные методы уже не обеспечивают необходимых точностей измерений.
В данной работе авторами проведены исследования влияния внешних факторов на точность измерений прибора атомно-эмиссионной спектроскопии.
...
16 04 2026 2:45:52
 Статья в формате PDF
134 KB...
Статья в формате PDF
134 KB...
15 04 2026 18:18:37
 Статья в формате PDF
160 KB...
Статья в формате PDF
160 KB...
14 04 2026 16:54:21
Еще:
Поддержать себя -1 :: Поддержать себя -2 :: Поддержать себя -3 :: Поддержать себя -4 :: Поддержать себя -5 :: Поддержать себя -6 :: Поддержать себя -7 :: Поддержать себя -8 :: Поддержать себя -9 :: Поддержать себя -10 :: Поддержать себя -11 :: Поддержать себя -12 :: Поддержать себя -13 :: Поддержать себя -14 :: Поддержать себя -15 :: Поддержать себя -16 :: Поддержать себя -17 :: Поддержать себя -18 :: Поддержать себя -19 :: Поддержать себя -20 :: Поддержать себя -21 :: Поддержать себя -22 :: Поддержать себя -23 :: Поддержать себя -24 :: Поддержать себя -25 :: Поддержать себя -26 :: Поддержать себя -27 :: Поддержать себя -28 :: Поддержать себя -29 :: Поддержать себя -30 :: Поддержать себя -31 :: Поддержать себя -32 :: Поддержать себя -33 :: Поддержать себя -34 :: Поддержать себя -35 :: Поддержать себя -36 :: Поддержать себя -37 :: Поддержать себя -38 ::