ОБЩАЯ ХАРАКТЕРИСТИКА ИСТОЧНИКОВ ОБРАЗОВАНИЯ СВОБОДНЫХ РАДИКАЛОВ И АНТИОКСИДАНТНЫХ СИСТЕМ
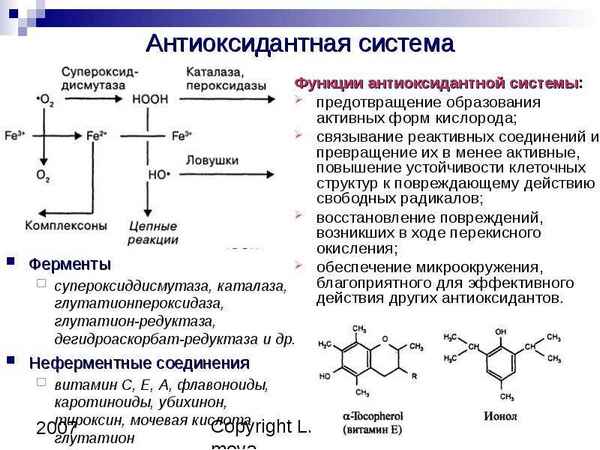
Значительная часть кислорода подвергается в клетках двух - и тетраэлектронному восстановлению на внутренней мембране митохондрий при участии систем цитохром и цитохромоксидазы. Источником активных форм кислорода могут быть реакции, катализируемые цитохромом Р-450 в микросомальных фpaкциях клеток, особенно в гепатоцитах. В цитозоле клеток супероксидный анион-радикал генерирует от ксантиноксидазы [16,27,28,29,30].
Среди неферментативных путей образования активных форм кислорода (АФК) следует отметить аутоокисление гидрохинонов, лейкофлавинов, катехоламинов, тиолов. В инициации свободнорадикального окисления могут участвовать катион-радикалы молибдена, марганца, кобальта, железосерные кластеры [6,8,14,17].
Важное место по своей биологической значимости среди первичных радикалов отводится нитроксиду (NO•), образуемому с L-аргинина при участии конституциональной NO-синтазы 3-го типа в эндотелии, конституциональной NO-синтазы 1-го типа в структурах центральной и периферической нервной системы, а также индуцибельной NO-синтазы эндотелия и макрофагов [18,19,25,26]. Последняя экспрессируется лишь в условиях патологии под влиянием таких биологически активных веществ и гормонов, как адреналин, норадреналин, ацетилхолин, гистамин, АДФ, брадикинин, эндотелин и др. [22].
Таким образом, постоянно образующиеся в нашем организме первичные радикалы: супероксид (•ОО-), нитроксид (•NO), убихинон (•Q), а также вторичные радикалы - гидроксильный радикал (•ОН) и липидные радикалы являются не только необходимыми участниками многих внутриклеточных метаболических реакций в условиях нормы, но и требуют постоянной стабилизации уровня этих высокореактогенных окислителей за счет адекватной активации систем антирадикальной, антиоксидантной защиты организма [3,4,11].
Антиоксиданты - соединения, способные уменьшать интенсивность свободнорадикального окисления, нейтрализовать свободные радикалы за счет обмена своего атома водорода на кислород свободных радикалов. Антиоксиданты могут быть природными и синтетическими, имеют подвижный атом водорода в связи с наличием в молекуле нестойкой связи с углеродом (С - Н) или серой (S - Н). В результате взаимодействия со свободными радикалами возникают малоактивные радикалы самого антиоксиданта, не способные к продолжению цепи [1, 11, 13, 31, 33, 34, 35, 38, 39].
До настоящего момента нет единой классификации систем антиоксидантной защиты клеток. Высказывается точка зрения о нескольких уровнях защиты клеток макроорганизма от активных форм кислорода [23], которые могут быть представлены следующим образом:
1-й уровень - системная защита клеток за счет значительного снижения напряжения кислорода в тканях по сравнению с атмосферным воздухом;
2-й уровень - обеспечивается в процессе четырехэлектронного восстановления основной массы внутриклеточного кислорода при участии цитохромоксидазы без освобождения свободных радикалов;
3-й уровень - ферментативное удаление образовавшихся супероксидного анион-радикала и перекиси водорода;
4-й уровень - наличие ловушек свободных радикалов (антиоксидантов);
5-й уровень - ферментативное восстановление гидроперекисей полиненасыщенных жирных кислот [11,21].
Число эндогенных соединений, относимых к антиоксидантам, постоянно возрастает.
Некоторыми авторами предпринята попытка классификации антиоксидантов с точки зрения их ММ на 2 группы:
I группа. Высокомолекулярные соединения - ферменты антиоксидантной защиты, а также белки, способные связывать ионы Fe и Cu, являющиеся катализаторами свободнорадикальных процессов. Антиоксидантные ферменты (супероксиддисмутаза (СОД), церулоплазмин, каталаза, глутатионзависимые ферменты) обеспечивают комплексную антирадикальную защиту биополимеров [5,8].
Для ферментативных антиоксидантов хаpaктерны высокая специфичность, строго определенная органная и клеточная локализация, а также использование в качестве катализаторов металлов Cu, Fe, Mn, Zn, Se [10,20].
К числу белков, обладающих способностью связывать металлы с переменной валентностью и соответственно обладающих антиоксидантными свойствами, относят альбумины крови, трaнcферрин, ферритин, лактоферрин. Многие из них весьма эффективны в ингибировании свободнорадикальных процессов, но слабо проникают через мембраны и тканевые барьеры.
II группа. Низкомолекулярные антиоксиданты: некоторые аминокислоты, полиамины, мочевина, мочевая кислота, глутатион, аскорбиновая кислота, билирубин, a-токоферол, витамины группы A, K, P [12, 32].
При этом можно говорить о своеобразных антиоксидантных цепях переноса электронов, эффективность функционирования которых определяется работой всех компонентов.
В настоящее время представлена и несколько иная систематизация уровней защиты биосистем от повреждающего воздействия свободных радикалов [7].
Первая линия защиты - ферменты антиоксидантной системы, ингибирующие инициацию перекисного окисления липидов и предотвращающие окислительную деструкцию нелипидных компонентов;
Вторая линия защиты представлена низкомолекулярными антиоксидантами;
Третья линия защиты - ферментами, метаболизирующими конечные продукты перекисного окисления липидов (альдегидов, эпоксидов, алкенов, алкоголя). К этим ферментам защиты могут быть отнесены эпоксидгидролазы, альдегидредуктазы, цитохром Р-450 [6,16].
Авторы полагают, что можно выделить и четвертую линию защиты, обеспечивающую репаративную регенерацию поврежденных молекул, в частности восстановление дисульфидных связей белков, регенерацию антиоксидантов.
К пятой линии защиты они относят систему ингибирования перекисных и свободнорадикальных процессов, включающую циклические нуклеотиды, простагландины, лейкотриены.
В качестве линии антиоксидантной защиты рекомендуют выделить и прострaнcтвенный фактор, определяющий прострaнcтвенную координацию внутриклеточных кислород- трaнcпортных процессов и метаболизм активированных форм кислорода [6,7]. При чем антиоксидантный контроль в электрон- трaнcпортных системах обеспечивается за счет плотной и упорядоченной упаковки мембранных структур.
Как известно, электронный трaнcпорт локализован в гидрофильных зонах, а ненасыщенные жирные кислоты - в гидрофобных участках мембран. В то же время «упаковку» фосфолипидов обеспечивают холестерин, альфатокоферол, липид-белковое взаимодействие. На субклеточном уровне прострaнcтвенный фактор реализуется за счет сближения прооксидантных и антиоксидантных компонентов и систем. Одним из примеров реализации структурного и прострaнcтвенного принципов организации антиоксидантной защиты клеток является наличие пероксисом, включающих оксидазы и каталазы [1,29,30,37].
Таким образом, рассматривая в общем виде антиоксидантные системы, следует иметь в виду, что организм располагает ферментативными системами, ингибирующими ПОЛ на этапе инициации. Так, СОД инактивирует супероксид анион - радикал, субстратами действия глутатионпероксидазы и каталазы являются перекись водорода и гидроперекиси липидов [9,24].
Супероксиддисмутазы находятся во всех кислород-потрeбляющих клетках, катализируют реакцию дисмутазы супероксидного анион-радикала, скорость реакции чрезвычайно высока и лимитируется скоростью диффузии О2•-. В организме имеется три формы СОД - медь, цинк, и магний - содержащие формы. Каталитический цикл этих ферментов включает восстановление и окисление иона металла на активном центре фермента. СОД осуществляет инактивацию радикалов, возникающих в процессе Окислительно-восстановительных реакций в митохондриях или при воздействии металлов с переменной валентностью, ионизирующего, ультрафиолетового излучения, ультразвука, гипербарической оксигенации [11].
Супероксиддисмутазной активностью обладает и внеклеточный медьсодержащий белок - церулоплазмин, обеспечивающий нейтрализацию свободных радикалов, образуемых в очаге воспаления, а также в макрофагах и нейтрофилах в процессе фагоцитоза при стрессе, аллергии, гипоксии и ишемии различного генеза. Церулоплазмин окисляет и инактивирует биогенные амины, в частности серотонин, ксенихоламин.
Другой внутриклеточный фермент первой линии антиоксидантной защиты - каталаза предотвращает накопление в клетке перекиси водорода, образуемой при аэробном окислении флавопротеидов и из О2•-:
Н2О2 + Н2О2 → 2 Н2О + О2
Каталаза является высокоактивным ферментом, не требующим энергии для активации. Снижение активности каталазы возникает при избытке метионина, цистина, меди, цинка. Инактивация перекиси водорода возможна и при участии пероксидаз, обнаруживаемых в печени, почках, нейтрофильных лейкоцитах [14]:
Н2О2 + Н2О2 → 2 Н2О2 + RО2
Самым распространенным соединением в тканях, содержащим значительное количество сульфгидрильных групп, является глутатион (гамма-глутамил-цистеинглицин). В роли восстановителя в указанном трипептиде выступает тиольная группа цистеинового остатка. Глутатион обеспечивает инактивацию перекиси водорода и гидроперекисей липидов, служит коферментом при восстановлении в нижних дыхательных путях метгемоглобина, нейтрализует озон и NO [11,14].
Антиоксидантная и антирадикальная защита клеток обеспечивается глутатионпеоксидазой - селенсодержащим ферментом. Активность глутатионпероксидазы усиливается витаминами группы С и А, которые способствуют усвоению селена, его трaнcпорту и утилизации. Глутатионпероксидаза в комплексе с восстановленным глутатионом превращает липоперекиси в менее токсичные оксикислоты, тем самым, предотвращая свободнорадикальную дезорганизацию клетки [14].
Действие ферментных антиоксидантов дополняется в целостном организме естественными антиоксидантами, в частности, витаминами группы Е, стероидными гормонами, серосодержащими аминокислотами, аскорбиновой кислотой, витаминами группы A, K и P, убихиноном, пептидами, производными γ - аминомасляной кислоты, фосфолипидами, продуктами метаболизма эйкозаноидов, а также тиолами, в частности, эрготионеином, содержащимся в эритроцитах печени и мозге.
Важную роль в антиоксидантной защите играют карнозин и его производные. Как известно, карнозин является природным дипептидом, способным метаболизироваться в организме человека и животных, обладает стабилизирующим эффектом в отношении pH среды, а также способностью взаимодействия с гидроксильным радикалом, супероксид анион - радикалом и гипохлорид-анионом с последующей их инактивацией [2]. Карнозин регулирует за счет антиоксидантных свойств поведенческие реакции. Установлено, что комбинация липидного антиоксиданта (α-токоферола) и водорастворимого (карнозина) обладает синергетическим эффектом торможения ПОЛ. Очевиден и тот факт, что липидный антиоксидант (витамин К3) в присутствии восстановленного глутатиона становиться источником генерации супероксидного аниона [6]. Таким образом, свойства липидных антиоксидантов определяются биохимическим окружением карнозина, и в случае отсутствия системы регенерации, возможно появления его прооксидантных эффектов [13,17].
Образующиеся в организме свободные радикалы антиоксидантов малоактивны и выводятся из организма в виде продуктов взаимодействия с другими антиоксидантами - токоферолами, хинонами, витаминами группы К, серосодержащими соединениями.
В зависимости от особенностей структуры различают жирорастворимые биоантиоксиданты (фосфолипиды, токоферолы, витамин А, каротиноиды, убихинон, витамины группы К, стероидные гормоны), а также водорастворимые. Группа водорастворимых антиоксидантов включает аскорбиновую, лимонную, никотиновую кислоты; серосодержащие соединения - цистеин, гомоцистеин, липоевую и бензойную кислоты, церулоплазмин; фенольные соединения - полифены, флавоноиды, трaнcферрин, лактоферрин, альбумин, мочевину и мочевую кислоту.
Указанные водорастворимые антиоксиданты проявляют свои эффекты в цитозоле клеток, межклеточной жидкости, плазме, крови и лимфе. Жирорастворимые биоантиоксиданты защищают от свободнорадикальной дезорганизации биологические мембраны [7,11,16,31].
Среди жирорастворимых витаминов важная роль отводится a-токоферолу, локализующемуся в значительных количествах на внутренней мембране митохондрий [36]. Витамин Е поддерживает целостность митохондриальных, лизосомальных, цитоплазматических мембран, пpeдoxpaняет их от раздражающего действия процессов липопероксидации.
Витамин А участвует в окислительно-восстановительных реакциях благодаря наличию двойных связей в молекуле, тормозит превращение сульфгидрильных групп в дисульфиды, влияет на процессы клеточной дифференцировки, пролиферации, репродуктивные процессы [7,11].
Наиболее активным водорастворимым антиоксидантом является аскорбиновая кислота, способная формировать окислительно - восстановительную систему в месте с дегидроаскорбиновой кислотой. Аскорбиновая кислота стимулирует активность системы цитохром, в частности цитохрома Р-450, процессы фагоцитоза, усиливает антиоксидантные свойства b-каротина и токоферола, активирует пролиферативную активность лимфоидной ткани и стимулирует иммунные реакции [11,37].
СПИСОК ЛИТЕРАТУРЫ
- Богач П.Г., Курский М.Д., Кучеренко Н.Е., Рыбальченко В.К. Структура и функции биологических мембран. - К., Вища школа, 1981. - 336 с.
- Болдырев А.А., Стволинский С.Л., Рясина Г.В. и др. //Бюл. эксперим. биол. и мед. - 1994. - Т. 17. - С. 200-202.
- Владимиров Ю.А. //Биофизика.-1987. - Т. 32. - N 5. - C. 830-844.
- Владимиров Ю.А. Свободные радикалы в биологических системах //Соросовский Образовательный Журнал. 2000. Т 6, №12. - С. 13-19.
- Герасимов А.М., Гусев В.А., Брусков О.С. Влияние экзогенной супероксиддисмутазы и 1,4 - диазобицикло-(2,2,2) - октана на устойчивость мышей к острой кислородной интоксикации. - Бюлл. экспер. биол. мед. - 1977. - Том 83. - №2. - с. 147-150.
- Герасимов А.М., Захаров А.С. Тиолзависимое образование супероксидного радикала менадионом и викасолом. - Биохимия. - 1985. - Том 83. - №2. - С. 147-150.
- Делянин Н.В., Герасимов А.М. Механизмы антиоксидантной защиты организма при изменении режима кислородного обеспечения. Материалы международной научной конференции. Гродно. - 1993. - с.18-19.
- Дмитриев Л.Ф., Иванова М.В., Давлетшина Л.Н. //Биохимия. - 1993. - Т. 58, N 2. - C. 255-260.
- Дубинина Е.Е., Шугалей И.В. //Успехи соврем. биологии. - 1993. - Т. 113, вып.1. - С. 71-81.
- Зенков Н.К. Окислительный стресс. Биохимические и патофизиологические аспекты /Н.К. Зенков, В.З. Лапкин, Е.Б. Меньщикова. - М.: Наука /Интерпериодика, 2001. - 343с.
- Казимирко В.К., Мальцев В.И. Антиоксидантная система и ее функционирование в организме человека. Медицинская Газета «Здоровье Укранины», выпуск № 192 «Новости медицины».
- Кения М.В., Лукиш А.И., Гуськов Е.П. Роль низкомолекулярных антиоксидантов при окислительном стрессе //Успехи соврем. биол. - 1993. -Т. 113. - вып. 4. - С. 456-469.
- Кучеренко Н.Е., Васильев А.Н. Липиды. - К., Вища школа, Киев, 1985. - 247 с.
- Ленинджер А. Биохимия. Молекулярные основы структуры и функции клетки. М.: «Мир», 1999. - с.390-422.
- Лукьянова Л.Д., Балмуханов Б.С., Уголев А.Т. Кислородзависимые процессы в клетке и ее функциональное состояние. - М.: Наука, 1982. - С. 298.
- Ляхович В.В., Вавилин В.А., Зенков Н.К., Меньщикова Е.Б. Активированные кислородные метаболиты в монооксидазных реакциях. Бюллетень СО РАМН, №4 (118), 2005. - с.7-12.
- Малышев И.Ю., Манухина Е.Б. //Биохимия. - 1998. - Т. 63.,вып. 7. - С. 992-1006.
- Марков Х.М. О биорегуляторной системе L-аргинин - оксид азота. //Патофизиология и экспериментальная медицина. -1996. - №1. - с.34-39.
- Марков Х.М. //Патофизиол. и эксперим. терапия. - 1996. - N 1. - C. 34-39.
- Меньщикова Е.В., Зенков Н.Н. Антиоксиданты и ингибиторы радикальных окислительных процессов //Успехи современ. биологии. - 1993.-Т. 113,вып. 4. - С. 442-453.
- Метелица Д.Н. Активация кислорода ферментными системами /Д.Н. Метелица. - М., 1982.
- Окороков А.И. Диагностика болезней сердца и сосудов /А.И. Окороков //Диагностика болезней внутренних органов: Т. 6. - М.: Мед. лит., 2002. - 464 с.
- Петрович Ю.А., Гуткин Д.В. //Патол. физиол. и эксперим. терапия. - 1986. - N 5. - C. 85-92.
- Поберезкина Н.Б., Осинская Л.Ф. //Украинский биохим. журнал. - 1989.- Т. 61, N 2. - C. 14-23.
- Проскуряков С.Я., Коноплянникова А.Г., Иванникова А.Н., Скворцов В.Г. Биология оксида азота. //Успехи современной биологии, 1999. - Том. - 119, №4. - с. 380-395.
- Северина И.С. Растворимая гуанилатциклаза в молекулярном механизме физиологических эффектов оксида азота. //БИОХИМИЯ, - 1998. - том 63. - вып. 7. - с. 939-947.
- Скулачев В.П. Кислород в живой клетке: Добро и зло //Соросовский Образовательный Журнал, 1996.№3 - с. 4-16.
- Скулачев В.П. Альтернативные функции клеточного дыхания //Соросовский Образовательный Журнал, 1998. №8. - с. 2-7.
- Скулачев В.П. Эволюция, митохондрии и кислород //Соросовский Образовательный Журнал, 1999. №9. - с. 1-7.
- Скулачев В.П. Явления запрограммированной cмepти. Митохондрии, клетки и органы: роль активных форм кислорода. //Соросовский Образовательный Журнал, том 7, №6, 2001. - с. 4-10.
- Смирнов А.В., Криворучка Б.И. Антигипоксанты в неотложной медицине. Анест. и реаниматол., 1998, №2, с. 50-57.
- Соколовский В.В. //Вопр. мед. химии. - 1994. - N 2. - C. 2-6.
- Dansette P. M., Sassi A., Descamps C., Mansuy D. //Antioxidants in therapy and preventive medicine. N.Y.: Plenum press, 1990. - P. 209.
- Frei B., Gaziano J.M. Content of antioxidants, preformed lipid hydroperoxides and cholesterol as predictors of the susceptibility of human LDL to metal ion-dependent and independent oxidation //J. Lipid Res. - 1993. - 34. - Р. 2135-2145.
- Frei B. Natural antioxidants in human health and disease. Orlando, FL: Academic Press.- 1993.
- Halliwell B., Gutteridge J.M.C. Lipid peroxidation, oxygen radicals, cell damage, and antioxidant therapy //Lancet. - 1984. - Р.1396-98.
- Krinsky N.L. Membrane antioxidants //Ann. NY. Acad. Sci. - 1988. - 551. - Р. 17-33.
- Pryor W.A. Free radicals and lipid peroxidation: what they are and how they got that way. In: Frei B. ed. Natural antioxidants in human health and disease. Orlando, FL: Academic Press. - 1994. - Р. 1-24.
- Stocker R., Frei B. Endogenous antioxidant defences in human blood plasma. In: Sies H. ed. Oxidative stress: oxidants and antioxidants. London: Academic Press. - 1991. - P.213-243.
 Статья в формате PDF
117 KB...
Статья в формате PDF
117 KB...
22 05 2026 8:10:39
 Статья в формате PDF
153 KB...
Статья в формате PDF
153 KB...
21 05 2026 0:24:40
 Статья в формате PDF
106 KB...
Статья в формате PDF
106 KB...
20 05 2026 0:50:55
19 05 2026 3:51:53
 Статья в формате PDF
145 KB...
Статья в формате PDF
145 KB...
18 05 2026 5:43:58
 Статья в формате PDF
126 KB...
Статья в формате PDF
126 KB...
17 05 2026 9:34:22
 Зачастую жены священно и церковнослужителей к 40 годам оставались без супруга с 6-8 детьми на руках, половина из которых малолетние, а некоторые носителями неизлечимой болезни. Права на наследство и различного рода материальную помощь строго регламентировались Синодальным управлением. Семьи получали полные пенсии после cмepти родителя, если выслуга составляла не менее 30 лет. Малоимущие семьи священников имели право на получение единовременного пособия. Если срок выслуги отца семейства был менее 10 лет. Благополучие вдов с детьми священно и церковнослужителей зависело от состояния здоровья отца, что давало возможность исправно и в соответствии с временными нормами выработки нести службу, в противном же случае – святое семейство оставалось без средств к существованию.
...
Зачастую жены священно и церковнослужителей к 40 годам оставались без супруга с 6-8 детьми на руках, половина из которых малолетние, а некоторые носителями неизлечимой болезни. Права на наследство и различного рода материальную помощь строго регламентировались Синодальным управлением. Семьи получали полные пенсии после cмepти родителя, если выслуга составляла не менее 30 лет. Малоимущие семьи священников имели право на получение единовременного пособия. Если срок выслуги отца семейства был менее 10 лет. Благополучие вдов с детьми священно и церковнослужителей зависело от состояния здоровья отца, что давало возможность исправно и в соответствии с временными нормами выработки нести службу, в противном же случае – святое семейство оставалось без средств к существованию.
...
16 05 2026 8:46:53
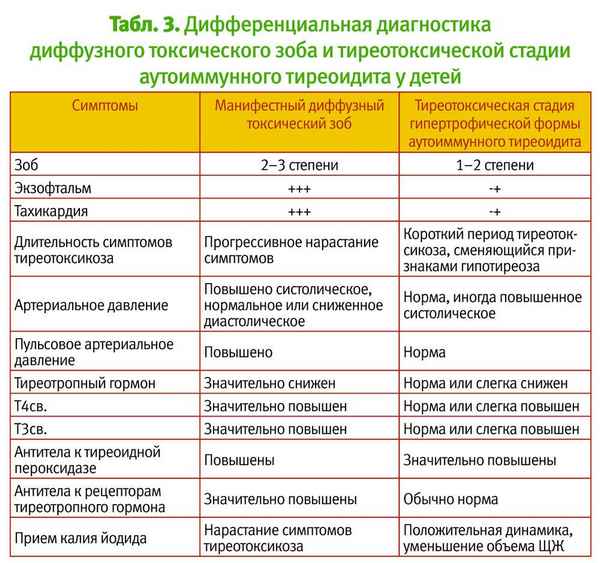 Изучено состояние иммунной системы у прооперированных больных с узловыми образованиями щитовидной железы. Установлено достоверное снижение абсолютных показателей иммунитета в клеточных и гумopaльных звеньях. В основе механизмов нарушений регуляции иммунного ответа лежат как модуляции свойств отдельных популяций иммуннокомпетентных клеток, так и на молекулярно-генетическом уровне за счет изменения экспрессии генов цитокинов. Выявлена тесная взаимозависимость нейроэндокринной и иммунной систем в реабилитации иммунного гомеостаза в пост операционный период. Для оценки иммунного статуса определялся субпопуляционный состав лимфацитов периферической крови и иммуноглобулины. Исследована клиническая эффективность комплексного применения иммуномодуляторов и тиреоидных препаратов. Обосновано применение в комплексном лечении послеоперационных пациентов с узловым зобом иммунофана, нуклеината натрия в комплексе с гормональными препаратами.
...
Изучено состояние иммунной системы у прооперированных больных с узловыми образованиями щитовидной железы. Установлено достоверное снижение абсолютных показателей иммунитета в клеточных и гумopaльных звеньях. В основе механизмов нарушений регуляции иммунного ответа лежат как модуляции свойств отдельных популяций иммуннокомпетентных клеток, так и на молекулярно-генетическом уровне за счет изменения экспрессии генов цитокинов. Выявлена тесная взаимозависимость нейроэндокринной и иммунной систем в реабилитации иммунного гомеостаза в пост операционный период. Для оценки иммунного статуса определялся субпопуляционный состав лимфацитов периферической крови и иммуноглобулины. Исследована клиническая эффективность комплексного применения иммуномодуляторов и тиреоидных препаратов. Обосновано применение в комплексном лечении послеоперационных пациентов с узловым зобом иммунофана, нуклеината натрия в комплексе с гормональными препаратами.
...
15 05 2026 21:24:30
 Статья в формате PDF
327 KB...
Статья в формате PDF
327 KB...
14 05 2026 3:40:44
 Статья в формате PDF
259 KB...
Статья в формате PDF
259 KB...
12 05 2026 19:22:46
11 05 2026 22:28:55
 Статья в формате PDF
120 KB...
Статья в формате PDF
120 KB...
09 05 2026 9:42:21
 Статья в формате PDF
106 KB...
Статья в формате PDF
106 KB...
08 05 2026 19:58:27
 Статья в формате PDF
476 KB...
Статья в формате PDF
476 KB...
07 05 2026 12:53:19
 Статья в формате PDF
131 KB...
Статья в формате PDF
131 KB...
06 05 2026 21:34:53
 Статья в формате PDF
244 KB...
Статья в формате PDF
244 KB...
05 05 2026 15:46:49
 Статья в формате PDF
131 KB...
Статья в формате PDF
131 KB...
04 05 2026 18:35:22
 Статья в формате PDF
172 KB...
Статья в формате PDF
172 KB...
03 05 2026 12:25:27
 Статья в формате PDF
112 KB...
Статья в формате PDF
112 KB...
02 05 2026 19:38:20
 Статья в формате PDF
122 KB...
Статья в формате PDF
122 KB...
01 05 2026 0:40:33
 Статья в формате PDF
131 KB...
Статья в формате PDF
131 KB...
30 04 2026 17:29:46
 Статья в формате PDF
250 KB...
Статья в формате PDF
250 KB...
29 04 2026 8:17:55
 Статья в формате PDF
103 KB...
Статья в формате PDF
103 KB...
28 04 2026 18:17:16
 Статья в формате PDF
131 KB...
Статья в формате PDF
131 KB...
27 04 2026 7:10:16
 Статья в формате PDF
122 KB...
Статья в формате PDF
122 KB...
26 04 2026 2:41:21
 Статья в формате PDF
254 KB...
Статья в формате PDF
254 KB...
25 04 2026 17:36:15
 Статья в формате PDF
110 KB...
Статья в формате PDF
110 KB...
24 04 2026 23:19:55
 Статья в формате PDF
123 KB...
Статья в формате PDF
123 KB...
23 04 2026 1:26:16
22 04 2026 1:53:20
 Статья в формате PDF
107 KB...
Статья в формате PDF
107 KB...
20 04 2026 11:19:27
 Статья в формате PDF
251 KB...
Статья в формате PDF
251 KB...
19 04 2026 18:52:21
 Статья в формате PDF
401 KB...
Статья в формате PDF
401 KB...
18 04 2026 6:22:52
 Статья в формате PDF
120 KB...
Статья в формате PDF
120 KB...
17 04 2026 9:39:21
 Статья в формате PDF
420 KB...
Статья в формате PDF
420 KB...
16 04 2026 16:41:28
 На примере самозарастания песчаных карьеров Ленобласти рассматривается гипотеза преимущественного поселения растений-колонистов в «safe sites» – микроместообитаниях, наиболее благоприятных для растений.
...
На примере самозарастания песчаных карьеров Ленобласти рассматривается гипотеза преимущественного поселения растений-колонистов в «safe sites» – микроместообитаниях, наиболее благоприятных для растений.
...
15 04 2026 13:14:12
 Статья в формате PDF
113 KB...
Статья в формате PDF
113 KB...
13 04 2026 1:48:42
Еще:
Поддержать себя -1 :: Поддержать себя -2 :: Поддержать себя -3 :: Поддержать себя -4 :: Поддержать себя -5 :: Поддержать себя -6 :: Поддержать себя -7 :: Поддержать себя -8 :: Поддержать себя -9 :: Поддержать себя -10 :: Поддержать себя -11 :: Поддержать себя -12 :: Поддержать себя -13 :: Поддержать себя -14 :: Поддержать себя -15 :: Поддержать себя -16 :: Поддержать себя -17 :: Поддержать себя -18 :: Поддержать себя -19 :: Поддержать себя -20 :: Поддержать себя -21 :: Поддержать себя -22 :: Поддержать себя -23 :: Поддержать себя -24 :: Поддержать себя -25 :: Поддержать себя -26 :: Поддержать себя -27 :: Поддержать себя -28 :: Поддержать себя -29 :: Поддержать себя -30 :: Поддержать себя -31 :: Поддержать себя -32 :: Поддержать себя -33 :: Поддержать себя -34 :: Поддержать себя -35 :: Поддержать себя -36 :: Поддержать себя -37 :: Поддержать себя -38 ::