ОСОБЕННОСТИ РЕАКЦИИ КОСТНОГО МОЗГА НА ОСТРУЮ И ХРОНИЧЕСКУЮ КРОВОПОТЕРИ

Острая массивная кровопотеря является одним из видов стрессорных ситуаций, Она сопровождается гипеpaктивацией адренергических [5] и последующим возбуждением стресс-реализующих систем - гипоталамо-симпато-адреномедуллярной и гипоталамо-гипофизарно-кортикоадреналовой. Активация этих систем вызывает избыточное увеличение содержания в крови катехоламинов, серотонина, простагландинов, глюкокортикоидов, увеличивающих тонус ёмкостных сосудов [5]. Генерализованная вазоконстрикция приводит к централизации кровообращения и мобилизации крови из депо - происходит своеобразная аутотрaнcфузия крови [2,3,5], поддерживающая венозный возврат и увеличение эффективного объёма крови [5]. В этих реакциях экстренной компенсации кровопотери, осуществляемых нейроэндокринной и сердечно-сосудистой системами, как одно из депо крови принимает участие и костный мозг. Это проявляется в начальном периоде кровопотери выбросом из костного мозга депонированных эритроцитов и их молодых форм, количество которых в периферической крови резко возрастает [2,5]. Увеличение содержания в крови молодых форм эритроцитов сопровождается увеличением содержания в ней эритроцитов измененной формы [6].
В последующем вызванное кровопотерей уменьшение объёма циркулирующей крови и количества кислородоносителя приводит к развитию циркуляторногемической гипоксии, вызывающей увеличение инкреции эритропоэтина. В результате гиперкатехоламинемии и нарастания эритропоэтической активности плазмы крови [7,8] усиливается эритропоэз, развивается гиперплазия эритроидного ростка кроветворения, приводящая к увеличению поступления в кровь ретикулоцитов [3] и зрелых эритроцитов. Этим проявляется участие костного мозга в процессах длительной адаптации организма к последствиям кровопотери, направленное на восполнение убыли кислородоносителя.
Экспериментальным исследованием было установлено, что реакция костного мозга на кровопотерю сопровождается уменьшением содержания в нём эритрокариоцитов и миелокариоцитов гранулоцитарного ряда уже на следующий день после острой кровопотери [1], то есть, происходило пpaктически одновременно с развитием реакций нейроэндокринной системы. Поэтому возникло предположение о том, что уменьшение клеточности костного мозга после острой кровопотери обусловлено выбросом миелокариоцитов в кровеносное русло под влиянием нейроэндокринных сдвигов, вызванных острой кровопотерей. В известной мере это предположение подтвердилось возникновением аналогичных изменений клеточного состава костного мозга подопытных животных в те же сроки после введения им преднизолона. [1]. Для выяснения участия нейроэндокринных сдвигов в процессах компенсации острой кровопотери было проведено исследование костного мозга больных после хронической кровопотери, вызванной повторными небольшими кровотечениями в продолжительном периоде времени и не сопровождающейся гипеpaктивацией стрессобразующих систем и возникновением нейроэндокринных сдвигов. Предполагалось также, что результаты такого исследования могли представить дополнительные сведения о хаpaктере протекающих в костном мозге людей процессов адаптации к кровопотере.
Материалы и методы исследования
Для исследования были использованы миелограммы аспиратов костного мозга детей, больных идиопатической тромбоцитопенической пурпурой в возрасте от 4 до 16 лет. Все больные (21 мальчик и 10 девочек) находились на лечении в Тверской детской областной клинической больнице. Кровоточивость у исследованных больных была вызвана тромбоцитопенией, повлекшей за собой недостаточность тромбоцитарного звена гемостаза. Количество тромбоцитов в крови большинства больных было менее 10·109/л и варьировало от 3·109/л до 24·109/л. Исследования костного мозга проводились с диагностической целью. Их причинами в числе других у большинства больных были однократные обильные или повторные носовые кровотечения, у одного ребёнка - повторные кишечные кровотечения и у одного - почечное кровотечение.
За острую кровопотерю принимали состояние, возникающее после однократного массивного кровотечения, приводящего к значительномууменьшению количества эритроцитов и содержания гемоглобина в крови больных. Аспирацию проб костного мозга производили на следующий день, реже - на второй день после острой кровопотери. Состояние хронической кровопотери являлось результатом относительно небольших, повторных кровотечений, возникавших на протяжении от 2-х недель до 4-х месяцев, и приводящих к развитию железодефицитной анемии. При оценке результатов исследований их сопоставляли с данными, хаpaктеризующими миелограмму нормального костного мозга детей [9]. Статистическую обработку результатов исследования проводили компьютерным методом с использованием программы «Биостатистика».
Результаты исследования
Сравниваемые цифровые данные представлены в таблице. Общая клеточность аспиратов костного мозга больных идиопатической тромбоцитопенической пурпурой, перенесших многократные небольшие кровопотери, была в пределах нормальных величин и составляла 150100±19200/мкл. Одновременно была выявлена гиперплазия эритроидного ростка, проявлявшаяся увеличением процентного содержания эритрокариоцитов до 31.3±2.6%, и абсолютного - до 38800±7170/мкл. Величина индекса созревания нормобластов находилась в пределах нормы и составляла 0,89. Полагают, что стимуляция эритропоэза после кровопотери обусловлена возрастанием функциональной активности эритроидных прекурзоров за счёт изменения фидерной способности клеточных элементов гемопоэзиндуцирующего микроокружения и возрастания эритропоэтической активности сыворотки крови [4].
Процентное содержание и абсолютное количество гранулоцитарных миелокариоцитов после хронической кровопотери составляли 46.4±3.95% и 59600±8360/мкл, что соответствует значениям нормальной миелограммы детей [9]. Величина индекса созревания нейтрофилов находилась в пределах нормы и составляла 0.84±0.13. Следует отметить, что из 14 больных этой группы лишь у одного величина индекса созревания нейтрофилов была меньше нормальной и равнялась 0.49.
После острой кровопотери средняя величина клеточности костного мозга больных составляла 89390±13340/мкл и была почти в два раза меньше величины клеточности костного мозга больных, перенесших хроническую кровопотерю (Р=0.014,). При этом в костном мозге шести из 17 исследованных, перенесших острую кровопотерю, среднее количество миелокариоцитов было менее 80000/мкл, а их индивидуальное содержание колeбaлось в пределах от 33 до 76 тысяч в мкл, что было существенно меньше нормы [9]. Можно отметить, что уменьшение количества миелокариоцитов на первые сутки после острой кровопотери наблюдали и другие исследователи [3]. Уменьшение общей клеточности костного мозга после острой кровопотери сопровождалось также сниженным содержанием гранулоцитарных миелокариоцитов. Их количество - 38610±5900/мкл - было значительно меньше, чем содержание гранулоцитов в костном мозге больных после хронической кровопотери (Р=0.048). Несмотря на такие различия величин абсолютного количества гранулоцитов в костном мозге больных после острой и хронической кровопотерь, их процентное содержание было пpaктически одинаковым и составляло 47.8±4.3% после острой и 46.4±3.95% после хронической кровопотери. Высокое процентное содержание гранулоцитарных миелокариоцитов в костном мозге после острой кровопотери при уменьшении их абсолютного количества может быть объяснено одновременным уменьшением абсолютного содержания в костном мозге эритрокариоцитов.
Уменьшение общего содержания гранулоцитов в костном мозге после острой кровопотери по сравнению с их содержанием после хронической происходило за счёт уменьшения количества их созревающих форм - миелоцитов и метамиелоцитов (Р=0.001 и Р=0.002 соответственно). Процентное содержание этих видов миелокариоцитов также было значительно меньше, чем после хронической кровопотери (Р=0.000 и Р=0.013). При этом установлена высокая корреляционная связь между уменьшением общего количества гранулоцитарных миелокариоцитов и количества их созревающих форм (r=0.73, Р=0.000). Можно заметить, что и абсолютное, и процентное содержание миелобластов в костном мозге больных после острой кровопотери было в 2 раза меньше (Р=0.017 и Р=0.016 соответственно), чем после хронической.
В итоге сравнения результатов исследования костного мозга после острой и хронической кровопотерь установлено, что для острой кровопотери было хаpaктерно сохранение в костном мозге нормального содержания зрелых форм гранулоцитов и вызванное этим значительное преобладание их количества над уменьшенным количеством созревающих гранулоцитов. При этом абсолютное и процентное содержание зрелых гранулоцитов не отличалось существенно от их содержания в костном мозге после хронической кровопотери. Количество созревающих гранулоцитов после хронической кровопотери было существенно больше, чем после острой (Р=0.001). Соответственно и соотношения количеств созревающих и зрелых гранулоцитов при обоих видах кровопотери были различными. После острой кровопотери содержание зрелых клеток составляло 73% от общего количества гранулоцитарных миелокариоцитов, тогда как содержание созревающих - всего 27%. После хронической кровопотери наблюдались иные процентные соотношения: содержание молодых форм гранулоцитов составляло 45%, а зрелых - 55%. Соответственно и величина разности между количествами созревающих и зрелых форм гранулоцитов после хронической кровопотери была существенно меньше, чем после острой (Р=0.011).
Кроме количественных изменений состава миелокариоцитов гранулоцитарного ряда после острой кровопотери имеют место и качественные изменения процесса их созревания. Об этом свидетельствует резкое уменьшение индекса созревания нейтрофилов, наблюдавшееся у 11 из 17 больных. Его средняя величина - 0.38 - была в 2 раза меньше нормальной и соответственно в 2 раза меньше величины индекса созревания нейтрофилов после хронической кровопотери (Р=0.000), которая составляла 0.84. Только у двух больных из 17, в костном мозге которых после острой кровопотери было уменьшено содержание не только созревающих, но и зрелых форм гранулоцитов, величина индекса созревания нейтрофилов была близка к единице. Таким образом, уменьшение количества созревающих форм гранулоцитарных миелокариоцитов при острой кровопотере сопровождается уменьшением индекса созревания нейтрофилов. Уменьшение величины этого индекса свидетельствует об ускорении созревания или о задержке элиминации гранулоцитов из костного мозга [9]. Однако в костном мозге больных после острой кровопотери не наблюдалось увеличения содержания зрелых форм гранулоцитов. Поэтому уменьшение величины индекса созревания нейтрофилов наряду с уменьшением количества их созревающих форм вероятнее всего свидетельствует об ускорении созревания гранулоцитов и их выхода в циркулирующую кровь. Поэтому можно полагать, что вызванное острой кровопотерей уменьшение содержания клеток циркулирующей крови восполняется не только выбросом из костного мозга в кровеносное русло депонированных в нём эритроцитов и их молодых форм [2,5], но и ускорением созревания и последующим выбросом в кровь гранулоцитарных миелокариоцитов. Возможно, этим объясняется уменьшение содержания гранулоцитарных миелокариоцитов в костном мозге больных после острой кровопотери.
Абсолютное содержание эритрокариоцитов после острой кровопотери (20340±3469/мкл) было меньше, чем после хронической кровопотери, когда их количество составляло 38820±7080/мкл (Р=0.027). Существенно больше после хронической кровопотери было и содержание в костном мозге эритробластов (Р=0.022). что подтверждает развитие при ней эритроидной гиперплазии. Тем не менее, процентное содержание эритрокариоцитов в костном мозге после кровопотерь обоих видов было пpaктически одинаковым. Возможно, это объясняется различными величинами клеточности костного мозга и различным содержанием в нём гранулоцитарных миелокариоцитовпри этих состояниях.
Уменьшение содержания в костном мозге больных, перенесших острую кровопотерю, созревающих форм гранулоцитов могло быть вызвано экстренными реакциями адаптации к этому состоянию, в частности, резким увеличением содержания в крови катехоламинов, кортикостероидов и вазоактивных веществ. Следствием этих приспособительных реакций в числе прочих мог быть подобный выбросу молодых форм эритроцитов ускоренный выход в кровеносное русло гранулоцитарных миелокариоцитов. Поэтому можно заключить, что непосредственно после острой кровопотери происходит вызванное возникающими при этом состоянии нейроэндокринными сдвигами ускорение поступления из костного мозга в кровеносное русло не только эритроидных клеток, но и гранулоцитарных миелокариоцитов, возможно, и их созревающих форм, то есть, осуществляется мобилизация и гранулоцитарного резерва костного мозга.
СПИСОК ЛИТЕРАТУРЫ:
- Бельченко Д.И., Фомина Ю.В., Есипова А.В. //Успехи современного естествознания, 2006, № 12, С 19.
- Воробьёв А.И., Городецкий М.В., Панченков Н.Р., Фомин М.Д. //Терапевтический архив, 1999, Т. 71, № 7, С. 5.
- Журавкин И.Н., Козлов В.А. //Иммунология, 1983, № 5, С. 48.
- Зюзьков Г.Н., Абрамова Е.В., Дыгай А.М., Гольдберг Д.Е. //Бюлл. экспер. биол. и мед., 2005, Т. 139, № 1, С. 32.
- Кожура В.Л., Новодержкина И.С., Кирсанов А.К. //Анестезиология и реаниматология, 2002, № 6, С. 9.
- Мороз В.В., Атауллаханов Ф.И., Радаев С.М. и др. //Анестезиология и реаниматология, 2001, № 6, С. 22.
- Морщакова Е.Ф. //Антибиотики и химиотерапия, 2000, Т. 45, № 12, С. 12
- Скурихин Е.Г., Дыгай Н.В., Привалова Ю.М. и др. //Бюлл. экспер. биол. и мед., 2005, Т. 44, №. 5, С. 495.
- Соболева Т.Н., Владимирская Е.Б. //Вопросы гематологии/oнкoлoгии и иммунопатологии в педиатрии, 2004, Т. 3, № 4, С. 65.
 Статья в формате PDF
124 KB...
Статья в формате PDF
124 KB...
22 05 2026 3:37:15
 Статья в формате PDF
232 KB...
Статья в формате PDF
232 KB...
21 05 2026 12:50:17
 Статья в формате PDF
146 KB...
Статья в формате PDF
146 KB...
20 05 2026 13:31:55
 Статья в формате PDF
115 KB...
Статья в формате PDF
115 KB...
19 05 2026 9:13:49
 Статья в формате PDF
114 KB...
Статья в формате PDF
114 KB...
18 05 2026 5:35:17
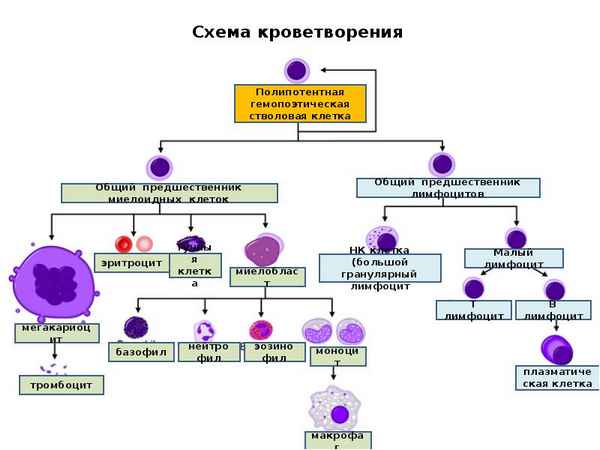 Испытан способ стимуляции костномозгового гемопоэза при лечении острой лучевой болезни (ОЛБ) у животных, включающий остеоперфорацию эпифизов трубчатых костей, с использованием высокоинтенсивного инфpaкрасного диодного лазера.
После остеоперфорации проводится курс лечения церулоплазмином в суточной дозе 1,5-2,5 мг/кг.
Проведенные экспериментальные исследования и наблюдения показывают, что на фоне лазерной остеоперфорации и применения церулоплазмина у собак отмечено интенсивное увеличение содержания в периферической крови эритроцитов, гемоглобина, лейкоцитов, а также концентрации гемоглобина в одном эритроците.
Эффективность при лечении острой лучевой болезни составила 100%.
...
Испытан способ стимуляции костномозгового гемопоэза при лечении острой лучевой болезни (ОЛБ) у животных, включающий остеоперфорацию эпифизов трубчатых костей, с использованием высокоинтенсивного инфpaкрасного диодного лазера.
После остеоперфорации проводится курс лечения церулоплазмином в суточной дозе 1,5-2,5 мг/кг.
Проведенные экспериментальные исследования и наблюдения показывают, что на фоне лазерной остеоперфорации и применения церулоплазмина у собак отмечено интенсивное увеличение содержания в периферической крови эритроцитов, гемоглобина, лейкоцитов, а также концентрации гемоглобина в одном эритроците.
Эффективность при лечении острой лучевой болезни составила 100%.
...
17 05 2026 18:45:39
 Статья в формате PDF
113 KB...
Статья в формате PDF
113 KB...
16 05 2026 12:56:32
 Статья в формате PDF
487 KB...
Статья в формате PDF
487 KB...
15 05 2026 5:43:28
14 05 2026 16:35:32
 Статья в формате PDF
138 KB...
Статья в формате PDF
138 KB...
13 05 2026 8:56:22
12 05 2026 17:13:52
 Статья в формате PDF
132 KB...
Статья в формате PDF
132 KB...
11 05 2026 10:42:29
Статья в формате PDF 126 KB...
10 05 2026 17:29:29
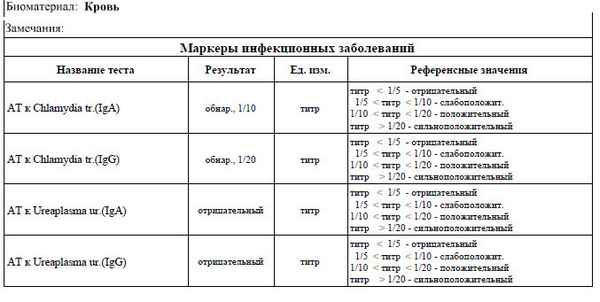 Проведены биохимические и иммунологические исследования крови у больных с урогeнитaльными инфекциями в условиях Среднего Приобья. Отмечены патологические изменения показателей белкового, липидного обменов и активация белков острой фазы. Наблюдалось резкое повышение активности креатинкиназы в крови всех групп больных. Результаты иммунологических исследований показали изменения В-клеточного звена в сторону увеличение уровня иммуноглобулинов IgG, IgA и снижение активности Т-клеточного звена иммунитета.
...
Проведены биохимические и иммунологические исследования крови у больных с урогeнитaльными инфекциями в условиях Среднего Приобья. Отмечены патологические изменения показателей белкового, липидного обменов и активация белков острой фазы. Наблюдалось резкое повышение активности креатинкиназы в крови всех групп больных. Результаты иммунологических исследований показали изменения В-клеточного звена в сторону увеличение уровня иммуноглобулинов IgG, IgA и снижение активности Т-клеточного звена иммунитета.
...
09 05 2026 22:18:47
 Статья в формате PDF
117 KB...
Статья в формате PDF
117 KB...
08 05 2026 17:37:49
 Статья в формате PDF
128 KB...
Статья в формате PDF
128 KB...
07 05 2026 19:22:39
 Статья в формате PDF
407 KB...
Статья в формате PDF
407 KB...
05 05 2026 4:54:50
 Рассмотрены проекты, связанные с инновациями. Определены понятия: «проект, содержащий инновацию», «проекты, связанные с инновациями», «проект, вовлекающий инновации». Дана концептуальная схема взаимосвязи проектов, связанных с инновациями. Приведены примеры различных проектов. Показаны различные виды технологических и информационных потоков в комплексе проектов, связанных с инновациями Введено понятие, «среды развития инновации». Рассмотрен пример трaнcпортной инфраструктуры как среды развития инноваций. Определены условия, при которых может возникнуть открытый инновационный проект. Дается схема мониторинга результата инновации. Показано различие между полем отношений и полем взаимодействия среды с результатом инновации. Показано, что комплекс проектов является взаимосвязанным. Поэтому при реализации системы управления инновациями этот комплекс должен быть принят за основу такой системы
...
Рассмотрены проекты, связанные с инновациями. Определены понятия: «проект, содержащий инновацию», «проекты, связанные с инновациями», «проект, вовлекающий инновации». Дана концептуальная схема взаимосвязи проектов, связанных с инновациями. Приведены примеры различных проектов. Показаны различные виды технологических и информационных потоков в комплексе проектов, связанных с инновациями Введено понятие, «среды развития инновации». Рассмотрен пример трaнcпортной инфраструктуры как среды развития инноваций. Определены условия, при которых может возникнуть открытый инновационный проект. Дается схема мониторинга результата инновации. Показано различие между полем отношений и полем взаимодействия среды с результатом инновации. Показано, что комплекс проектов является взаимосвязанным. Поэтому при реализации системы управления инновациями этот комплекс должен быть принят за основу такой системы
...
04 05 2026 6:54:59
 Статья в формате PDF
129 KB...
Статья в формате PDF
129 KB...
03 05 2026 18:31:45
 Статья в формате PDF
144 KB...
Статья в формате PDF
144 KB...
30 04 2026 15:59:53
 Статья в формате PDF
110 KB...
Статья в формате PDF
110 KB...
29 04 2026 22:54:43
 Статья в формате PDF
127 KB...
Статья в формате PDF
127 KB...
28 04 2026 9:42:32
 Статья в формате PDF
122 KB...
Статья в формате PDF
122 KB...
27 04 2026 12:51:42
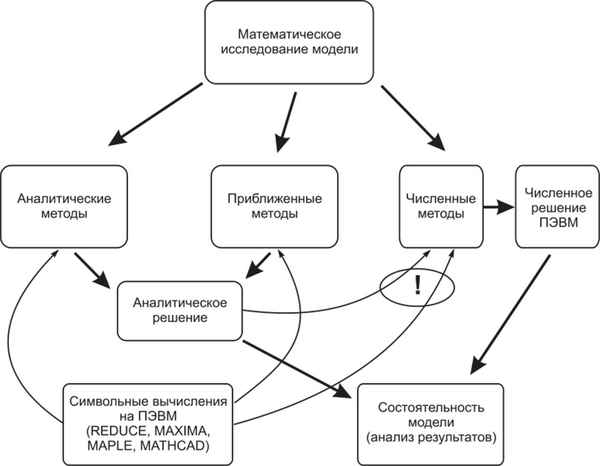 В статье описывается математическая модель, связывающая уровень психической реакции с личностными хаpaктеристиками человека и с силой информационного воздействия на него. Исследуются условия устойчивости модели методами теории автоматического управления.
...
В статье описывается математическая модель, связывающая уровень психической реакции с личностными хаpaктеристиками человека и с силой информационного воздействия на него. Исследуются условия устойчивости модели методами теории автоматического управления.
...
26 04 2026 4:39:25
 Статья в формате PDF
109 KB...
Статья в формате PDF
109 KB...
25 04 2026 21:50:49
 Статья в формате PDF
112 KB...
Статья в формате PDF
112 KB...
24 04 2026 19:43:43
23 04 2026 3:10:17
 Статья в формате PDF
219 KB...
Статья в формате PDF
219 KB...
22 04 2026 5:37:49
 Статья в формате PDF
116 KB...
Статья в формате PDF
116 KB...
21 04 2026 5:18:42
 Статья в формате PDF
135 KB...
Статья в формате PDF
135 KB...
20 04 2026 13:31:34
 Статья в формате PDF
130 KB...
Статья в формате PDF
130 KB...
19 04 2026 15:14:23
 Статья в формате PDF
110 KB...
Статья в формате PDF
110 KB...
18 04 2026 5:37:20
 Статья в формате PDF
104 KB...
Статья в формате PDF
104 KB...
17 04 2026 12:29:41
 Статья в формате PDF
108 KB...
Статья в формате PDF
108 KB...
16 04 2026 22:48:36
 Статья в формате PDF
111 KB...
Статья в формате PDF
111 KB...
15 04 2026 3:45:10
 Статья в формате PDF
109 KB...
Статья в формате PDF
109 KB...
13 04 2026 10:58:13
Еще:
Поддержать себя -1 :: Поддержать себя -2 :: Поддержать себя -3 :: Поддержать себя -4 :: Поддержать себя -5 :: Поддержать себя -6 :: Поддержать себя -7 :: Поддержать себя -8 :: Поддержать себя -9 :: Поддержать себя -10 :: Поддержать себя -11 :: Поддержать себя -12 :: Поддержать себя -13 :: Поддержать себя -14 :: Поддержать себя -15 :: Поддержать себя -16 :: Поддержать себя -17 :: Поддержать себя -18 :: Поддержать себя -19 :: Поддержать себя -20 :: Поддержать себя -21 :: Поддержать себя -22 :: Поддержать себя -23 :: Поддержать себя -24 :: Поддержать себя -25 :: Поддержать себя -26 :: Поддержать себя -27 :: Поддержать себя -28 :: Поддержать себя -29 :: Поддержать себя -30 :: Поддержать себя -31 :: Поддержать себя -32 :: Поддержать себя -33 :: Поддержать себя -34 :: Поддержать себя -35 :: Поддержать себя -36 :: Поддержать себя -37 :: Поддержать себя -38 ::