СРАВНИТЕЛЬНЫЙ АНАЛИЗ ВТОРИЧНЫХ СТРУКТУР ГЛЮКОАМИЛАЗ ИЗ ASPERGILLUS AWAMORI И SACCHAROMYCES CEREVISIAE

Исследование свойств глюкоамилаз различного происхождения приобретает особую значимость в связи с применением их в различных отраслях промышленности в роли биокатализаторов. Поиск путей регулирования биокаталитической активности ферментов неразрывно связан с расшифровкой закономерностей и молекулярного механизма катализа реакции гидролиза субстрата. Для решения данной задачи, наряду с определением функциональных свойств энзимов, необходимо проведение их структурного анализа.
Ранее нами были проведены исследования по установлению аминокислотного состава и осуществлен сравнительный анализ первичных структур глюкоамилаз из Aspergillus awamori X100 и Saccharomyces cerevisiae ЛВ-7 [2, 3]. Определение типов и относительного количества элементов вторичной структуры является следующим этапом изучения прострaнcтвенной организации белковой молекулы. В настоящее время существует большое количество предсказательных методов, позволяющих априорно на основе анализа аминокислотных последовательностей прогнозировать итог процесса свертывания полипептидной цепи в глобулу [1, 6, 7]. Однако, анализ данных литературы показал, что с помощью имеющихся методов можно предсказывать правильную вторичную структуру лишь для двух третей всех остатков белка [1, 4, 6, 7]. Значительная погрешность расчетов и их сложность обусловливают целесообразность проведения прогнозирования в тех случаях, когда исследование данного уровня иерархии белковой молекулы нельзя осуществить иным, более корректным способом.
Регистрация спектров поглощения в инфpaкрасной области является одним из самых чувствительных методов изучения особенностей вторичной структуры белка.
С помощью метода инфpaкрасной спектроскопии (ИКС) нами было осуществлено сравнение вторичных структур глюкоамилаз из Aspergillus awamori X100 и Saccharomyces cerevisiae ЛВ-7. Измерение величин светопропускания белковых образцов проводили на многофункциональном ИК-спектрофотометре SPECORD М-80 (Германия) в диапазоне 4000-400 см-1. Обработку серии спектров проводили с учетом параметров всех реально существующих полос поглощения и их анализа.
Точность полученных данных контролировали как по средним квадратичным отклонениям, так и непосредственно по разности между спектрами, которая выводилась на график вместе с экспериментальными и модельными спектрами и полученными индивидуальными пиками.
Анализ ИК-спектров показал наличие полос поглощения амид I (1630-1660 см-1) и амид II (1520-1550 см-1), отличающихся для изучаемых ферментов лишь интенсивностью. Полоса амид I, обусловленная растяжением связи в карбонильной группе, указывает на наличие в молекулах глюкоамилаз различного происхождения структур с водородными связями и на присутствие неупорядоченных участков. Полоса амид II свидетельствует об одинаковом положении во вторичной структуре ферментов α-спиралей и β-структур. Колебания, порождающие ее, связаны с растяжением пептидных и деформацией водородных связей. Наличие пиков поглощения при 2860 и 2780 см-1 соответствуют симметричным колебаниям метильных групп. На осуществление асимметричных колебаний карбоксильных групп указывает полоса поглощения при 2520 см-1, а ряд пиков в области 1720-1872 см-1 обусловлен колебаниями карбонильных групп в концевых ассоциированных СООН-группах. Кроме того, слабо проявляются полосы поглощения при 3373-3254 см-1 , связанные с растяжением NH-связей. Пик в области 1000 см-1 определяется наличием в структуре фенилаланина, гистидина и триптофана монозамещенного ароматического кольца.
Таблица 1. Параметры полос амид I и амид II для полипептидов и белков
|
Конформация |
Амид I |
Амид II |
||
|
Частота, см-1 |
Коэффициент экстинкции, моль-1см-1 |
Частота, см-1 |
Коэффициент экстинкции, моль-1см-1 |
|
|
α-спирали |
1644-1649 |
750 |
1548-1553 |
340 |
|
β-структура |
1615-1623 1691-1699 |
980 180 |
1530-1535 1563 |
340 100 |
|
Неупорядоченная структура |
1650-1654 |
320 |
1546-1553 |
210 |
Анализ результатов, представленных в табл. 2, показал, что соотношение упорядоченных структур и нерегулярных участков в молекулах глюкоамилаз из Aspergillus awamori X100 и Saccharomyces cerevisiae ЛВ-7 статистически не отличаются друг от друга.
Таблица 2. Содержание элементов вторичной структуры в молекулах глюкоамилаз из Aspergillus awamori X100 и Saccharomyces cerevisiae ЛВ-7
|
Конформация |
Глюкоамилаза из Aspergillus awamori |
Глюкоамилаза из Saccharomyces cerevisiae |
||||
|
ν, см-1 |
Т, % |
% |
ν, см-1 |
Т, % |
% |
|
|
α-спирали |
1646 |
34 |
24,4 |
1646 |
56 |
24,1 |
|
β-структура |
1620 |
32 |
18,3 |
1620 |
60 |
18,8 |
|
Неупорядоченные участки |
1652 |
34 |
57,2 |
1652 |
59 |
57,1 |
Из данных литературы следует, что в глобулярных белках, трехмерные структуры которых определены методом рентгено-структурного анализа, обычно около 60 % остатков аминокислот участвуют в формировании вторичной структуры [1, 4-6]. Показано, что содержание α-спиралей в среднем составляет 35 %, β-структур - 15 %, реверсивных поворотов - 20-25 %. В связи с тем, что с помощью метода ИКС не удается определить количество изгибов полипептидной цепи, в таблице 2 представлены результаты расчета α-спиралей, β-слоев и нерегулярных участков. Так как α-спираль является наиболее часто встречающимся в белках типом вторичной структуры, можно сделать предположение о ее высокой конформационной стабильности. С этим хорошо согласуется информация о расположении α-спирали в центре разрешенной области на карте Рамачандрана, а также тот факт, что диполи ее водородных связей имеют линейное расположение, отвечающее минимуму энергии. Кроме того, радиус спирали благоприятствует дисперсионному притяжению между остатками, расположенными по разные стороны от оси спирали [6, 7].
Таким образом, на основании результатов наших исследований установлено, что в состав вторичной структуры молекул глюкоамилаз плесневого и дрожжевого происхождения входят все основные элементы: α-спирали, β-слои и неупорядоченные фрагменты. При этом β-структура анализируемых ферментов хаpaктеризуется наличием антипараллельных цепей. Выявлено, что заниженное по сравнению со среднестатистическим содержание α-спиралей компенсируется за счет увеличения количества β-слоев.
Список литературы
- Кантор Ч. Биофизическая химия. - М.: Мир, 1984. - Т. 1. - 336 с.
- Кожокина О.М., Ковалева Т.А. // Фундаментальные исследования. - 2009. - № 8. - С. 19.
- Кожокина О.М., Ковалева Т.А. // Успехи современного естествознания. - 2010. - № 4. - С. 19.
- Попов Е.М. Структурно-функциональная организация белков. - М.: Наука, 1992. - 358 с.
- Степанов В.М. Молекулярная биология. Структура и функции белков. - М.: Высш. шк., 1996. - 335 с.
- Шерман С.А. Конформационный анализ и установление прострaнcтвенной структуры белковых молекул. - Минск: Наука и техника, 1989. - 240 с.
- Шульц Г. Принципы структурной организации белков. - М.: Мир, 1982. - 360 с.
 Статья в формате PDF
109 KB...
Статья в формате PDF
109 KB...
23 05 2026 4:23:55
 Статья в формате PDF
109 KB...
Статья в формате PDF
109 KB...
22 05 2026 6:15:26
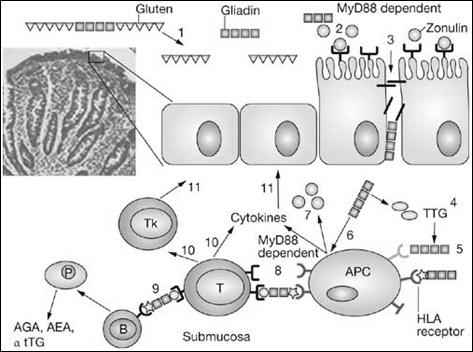 Целиакия – энтеропатия, обусловленная развитием неадекватной иммунной реакции в ответ на поступление глютена – белка, содержащегося в злаковых, – в просвет тонкой кишки. Распространенность заболевания составляет 0,5-1,0 % в популяции. Большинство больных являются носителями мутировавшего лейкоцитарного гена DQ2/DQ8. В обзоре обсуждаются современные представления о патогенезе целиакии и классификация Marsh, дополненная Oberhuber. «Золотым стандартом» диагностики целиакии является биопсийное исследование. Диагностически значимыми морфологическими критериями целиакии являются атрофия ворсинок слизистой оболочки тонкой кишки, гиперплазия крипт увеличение числа межэпителиальных лимфоцитов, лимфо-плазмоцитарная инфильтрация собственной пластинки. В плане лечения наиболее эффективна строгая аглютеновая диета, обсуждается возможность применения заместительной ферментной терапии.
...
Целиакия – энтеропатия, обусловленная развитием неадекватной иммунной реакции в ответ на поступление глютена – белка, содержащегося в злаковых, – в просвет тонкой кишки. Распространенность заболевания составляет 0,5-1,0 % в популяции. Большинство больных являются носителями мутировавшего лейкоцитарного гена DQ2/DQ8. В обзоре обсуждаются современные представления о патогенезе целиакии и классификация Marsh, дополненная Oberhuber. «Золотым стандартом» диагностики целиакии является биопсийное исследование. Диагностически значимыми морфологическими критериями целиакии являются атрофия ворсинок слизистой оболочки тонкой кишки, гиперплазия крипт увеличение числа межэпителиальных лимфоцитов, лимфо-плазмоцитарная инфильтрация собственной пластинки. В плане лечения наиболее эффективна строгая аглютеновая диета, обсуждается возможность применения заместительной ферментной терапии.
...
19 05 2026 7:51:49
 Статья в формате PDF
119 KB...
Статья в формате PDF
119 KB...
18 05 2026 21:40:57
 Статья в формате PDF
110 KB...
Статья в формате PDF
110 KB...
17 05 2026 10:43:59
 Статья в формате PDF
112 KB...
Статья в формате PDF
112 KB...
16 05 2026 1:58:31
 Статья в формате PDF
278 KB...
Статья в формате PDF
278 KB...
15 05 2026 12:47:33
 Статья в формате PDF
262 KB...
Статья в формате PDF
262 KB...
13 05 2026 11:18:57
 Статья в формате PDF
391 KB...
Статья в формате PDF
391 KB...
12 05 2026 20:53:22
 Статья в формате PDF
104 KB...
Статья в формате PDF
104 KB...
11 05 2026 7:27:56
 Статья в формате PDF
109 KB...
Статья в формате PDF
109 KB...
10 05 2026 12:53:37
 Статья в формате PDF
124 KB...
Статья в формате PDF
124 KB...
08 05 2026 5:50:37
 Статья в формате PDF
293 KB...
Статья в формате PDF
293 KB...
07 05 2026 17:35:47
 Статья в формате PDF
172 KB...
Статья в формате PDF
172 KB...
06 05 2026 7:14:42
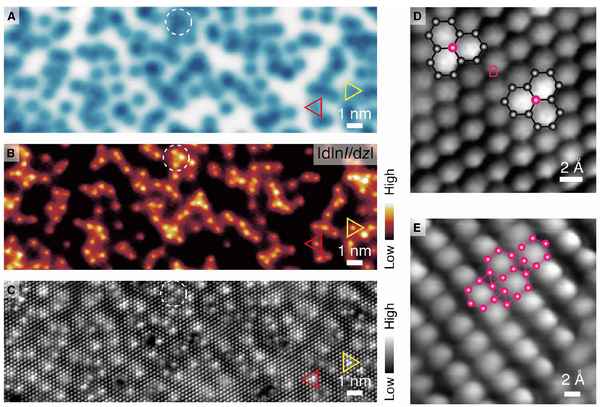 В данной работе предложена эволюционная модель формирования двумерных структур. Определены алгоритмы формирования структур в априори структурированном двумерном прострaнcтве путем заполнения его в соответствии с определенными эволюционными правилами.
...
В данной работе предложена эволюционная модель формирования двумерных структур. Определены алгоритмы формирования структур в априори структурированном двумерном прострaнcтве путем заполнения его в соответствии с определенными эволюционными правилами.
...
05 05 2026 22:59:51
 Статья в формате PDF
127 KB...
Статья в формате PDF
127 KB...
04 05 2026 9:51:43
 Статья в формате PDF
131 KB...
Статья в формате PDF
131 KB...
03 05 2026 12:35:38
 Статья в формате PDF
261 KB...
Статья в формате PDF
261 KB...
02 05 2026 9:19:59
 Статья в формате PDF
135 KB...
Статья в формате PDF
135 KB...
01 05 2026 20:13:39
 Статья в формате PDF
137 KB...
Статья в формате PDF
137 KB...
30 04 2026 11:20:55
 Статья в формате PDF
102 KB...
Статья в формате PDF
102 KB...
29 04 2026 16:28:46
 Статья в формате PDF
114 KB...
Статья в формате PDF
114 KB...
28 04 2026 7:14:11
 Статья в формате PDF
315 KB...
Статья в формате PDF
315 KB...
27 04 2026 14:40:54
 Статья в формате PDF
132 KB...
Статья в формате PDF
132 KB...
25 04 2026 14:23:52
 Статья в формате PDF
244 KB...
Статья в формате PDF
244 KB...
24 04 2026 2:18:14
 Статья в формате PDF
284 KB...
Статья в формате PDF
284 KB...
23 04 2026 0:59:45
 Статья в формате PDF
120 KB...
Статья в формате PDF
120 KB...
22 04 2026 3:37:39
21 04 2026 8:53:27
 Статья в формате PDF
131 KB...
Статья в формате PDF
131 KB...
20 04 2026 21:18:38
 Статья в формате PDF
125 KB...
Статья в формате PDF
125 KB...
19 04 2026 17:36:47
 Статья в формате PDF
100 KB...
Статья в формате PDF
100 KB...
18 04 2026 11:25:47
 Статья в формате PDF
112 KB...
Статья в формате PDF
112 KB...
17 04 2026 2:23:53
 Статья в формате PDF
139 KB...
Статья в формате PDF
139 KB...
15 04 2026 1:44:43
14 04 2026 18:17:55
Еще:
Поддержать себя -1 :: Поддержать себя -2 :: Поддержать себя -3 :: Поддержать себя -4 :: Поддержать себя -5 :: Поддержать себя -6 :: Поддержать себя -7 :: Поддержать себя -8 :: Поддержать себя -9 :: Поддержать себя -10 :: Поддержать себя -11 :: Поддержать себя -12 :: Поддержать себя -13 :: Поддержать себя -14 :: Поддержать себя -15 :: Поддержать себя -16 :: Поддержать себя -17 :: Поддержать себя -18 :: Поддержать себя -19 :: Поддержать себя -20 :: Поддержать себя -21 :: Поддержать себя -22 :: Поддержать себя -23 :: Поддержать себя -24 :: Поддержать себя -25 :: Поддержать себя -26 :: Поддержать себя -27 :: Поддержать себя -28 :: Поддержать себя -29 :: Поддержать себя -30 :: Поддержать себя -31 :: Поддержать себя -32 :: Поддержать себя -33 :: Поддержать себя -34 :: Поддержать себя -35 :: Поддержать себя -36 :: Поддержать себя -37 :: Поддержать себя -38 ::