ОБРАЗОВАНИЕ ГРАДИЕНТНЫХ ОКСИДНЫХ ПОКРЫТИЙ В МИКРОПЛАЗМЕННОМ РЕЖИМЕ

Введение
Разработка новых методов обработки алюминия и его сплавов импульсными токами большой плотности, которая приводит к образованию покрытий, обладающих высокой износостойкостью, механической прочностью, термостойкостью [1], связана с исследованием физико-химических закономерностей образования данных покрытий.
В данной работе дано математическое описание процесса образования градиентных оксидных покрытий в микроплазменном режиме для случая, когда лимитирующей стадией процесса является стадия доставки ионов из раствора электролита к поверхности электрода.
Методика эксперимента
При проведении электрохимических измерений использовали трехэлектродную электрохимическую ячейку, которая включала рабочий электрод, выполненный из сплава алюминия Д-16, электрод сравнения (стандартный платиновый электрод ЭПЛ-02) и вспомогательный электрод из нержавеющей стали. Для измерения значения токов, задающего, поляризующего напряжений был использован информационно-измерительный комплекс [2]. Для определения значения толщины покрытий применяли вихревой толщиномер ВТ-10НЦ. В качестве электролита использовали щелочной электролит (А), содержащий фосфаты, фториды, бораты щелочных металлов. Электролит готовили на дистиллированной воде из реактивов марки "ч.д.а", "х.ч.".
Теоретическая часть
Рассмотрим процессы, протекающие на поверхности электрода при прохождении анодно-катодного электрического тока. При прохождении анодной составляющей электрического на поверхности металла образуется оксидная пленка и происходят изменения концентрации ионов в приэлектродном слое. Образующаяся оксидная пленка и концентрационные изменения ионов в приэлектродном слое создают барьерный слой. Если напряженность на границе раздела металлраствор, создаваемая источником питания, выше чем электрическая прочность барьерного слоя, то возникает электрический пробой (микродуга). В "шнуре" микродуги за короткий промежуток времени развиваются высокие температура и давление, которые приводят к образованию паро-газовой среды в объеме. Газовая полость состоит из ионов кислорода, водорода, паров воды, причем анодная часть микродуги в основном состоит из ионов кислорода, которые диффундируют вглубь металла. Параллельно на электроде идут электрохимические реакции.
Микроплазменные разряды приводят к локальному плавлению металла основы, который выбрасывается в раствор дуговым процессом, где часть его гидратируется, а часть остается в ионной форме в растворе. Гидратированные ионы металла под воздействием высокой температуры переходят в оксиды. Образующиеся оксиды встраиваются в покрытие.
Рассмотрим модель образования градиентных оксидных покрытий, когда лимитирующей стадией процесса является диффузия ионов к поверхности электрода, и сделаем следующие приближения [3]:
1.Электрическое поле вблизи поверхности электрода не оказывает влияние на движение ионов
2.Скорость прямого перехода металла основы в оксид под действием микроплазменного процесса мала.
Распределение ионов кислорода, гидроксид-ионов, ионов металла на границе металл-оксид-раствор представлены на рис.1.
На границе x=0 происходит выделение кислорода, который диффундирует вглубь металла - зона (М), кривая 1 (рис.1).
Начальные и граничные условия описываются уравнениями (1):
(1)
где: СА - концентрация ионов кислорода, D - коэффициент диффузии, t -время, С0 - концентрация ионов кислорода на границе х=0 в любой момент времени.
Анализ распределения концентрации ионов кислорода на границе металл-раствор при граничных условиях (1) показал, что с увеличением времени обработки внедрение кислорода в металл повышается (рис. 2).
В пористом оксидном слое (О) в связи с низкой скоростью диффузии изменение концентрации анионов OH- остается постоянным во времени и линейно уменьшается от границы раздела металл-оксид до границы раздела оксид-раствор - зона О, кривая 2 (рис.1) и выражается следующим уравнением:
CВ (x, t) =Cbs-bx
0 < x < h (2),
где, СBS - поверхностная концентрация анионов OH- при х=0, b- коэффициент пропорциональности.
Распределение концентрации гидроксид-ионов OH- в растворе - зона (Р), кривая 3 (рис.1) описывается уравнениями:
(3)
где, ССо, ССS - соответственно объемная и поверхностная концентрации гидроксид ионов в приэлектродном слое a- коэффициент пропорциональности.
Поток гидроксид-ионов (анионов) будет определяться соотношением:
(4)
Распределение концентрации ионов металла СМ в приэлектродном слое - зона Р, кривая 4 (рис.1 ) описывается системой уравнений:
где, СоМ, СMS - соответственно объемная и поверхностная концентрация ионов металла в приэлектродном слое, К- константа химического равновесия. Поток ионов металла на границе оксид-раствор имеет вид:
(6)
Толщина покрытия зависит от потока гидроксид ионов и ионов металла и соотношения их в растворе.
1.При избытке в растворе анионов толщина покрытия зависит от величины коэффициента диффузии ионов металла DM , поверхностной, объемной концентрации ионов металла, времени процесса и определяется уравнением:
(7)
2.При избытке в растворе катионов металла толщина покрытия зависит от
величины коэффициента диффузии анионов DA , поверхностной, объемной концентрации анионов, времени процесса и описывается уравнением:
(8)
3.При эквивалентном соотношении концентраций анионов и катионов:
где, Сt, K1, K2, K3 - коэффициенты, учитывающие изменение состава, объема, массы металла при переходе его в оксид.
Экспериментальная часть
Согласно теоретическим положениям скорость образования покрытий (поток ионов) лимитируется процессом доставки и определяется природой электролита и природой металла. Экспериментально это подтверждается изменением плотности тока от длительности импульса. Для исследования потоков анионов предварительно готовили образец из Д-16. Для этого на образец наносили оксидный слой в микроплазменном режиме в электролите (А) при напряжении анодного импульса 350В в течение 300 секунд. Зависимость плотности максимума импульсного анодного тока от длительности импульса представлена на рис. 3. Величина плотности тока уменьшается с увеличением длительности импульса. Это связано с тем, что с увеличением длительности импульса, количество ионов в приэлектродном слое уменьшается, уменьшается градиент концентрации и, соответственно, плотность тока.
При расчете скорости роста покрытия толщину покрытия определяли уравнением 7, так как используемый нами электролит щелочной. Расчеты по теоретическим уравнениям связаны с определением величин Ct и Kn , где Kn =K1 ,K2 ,K3 . Эти величины зависят от состава и пористости покрытия. Поскольку теория пористости покрытий в процессе микроплазменной обработки в настоящее время не разработана, величину произведения СM ×Ct ×Kn =S можно определить из экспериментальных зависимостей и в дальнейшем использовать величину S как параметр при расчетах. Теоретические и экспериментальные зависимости толщины оксидного покрытия от времени в импульсном режиме представлены на рис. 4. Эксперименты проводились в электролите (А) в импульсном режиме при длительности импульса 200 мкс и частоте 50 Гц. При расчетах учитывали, что во время пауз между импульсами ток равен нулю.
Сравнение экспериментальной зависимости толщины покрытия от времени в импульсном режиме с теоретическими расчетами (рис. 4) показывает, что они удовлетворительно согласуются.
Рис.1. Схема градиентного оксидного покрытия;
1-распределение ионов кислорода в металле, 2-распределение концентрации гидроксид-ионов в окисном слое, 3-распределение концентрации гидроксид-ионов в приэлектродном слое, 4-распределение концентрации ионов металла в приэлектродном слое
Рис.2.Распределение концентрации ионов кислорода в металле
Рис.3. Экспериментальная зависимость плотности максимума импульсного анодного тока от длительности импульса.
Рис.4. Теоретическая зависимость толщины покрытия от времени t, полученная по уравнению 7 (кривая 1), при условии D = 10-5 см-2с-1, СМ = 1 г/см3, СMS = 0,01 г/см3, S=0,002; 2 - по уравнению h = A(i × t)n [4] в гальваностатических условиях n=0.45, Аi0,45=4 для импульсного процесса при длительности импульса 200мкс, частоте 50 Гц; 3- экспериментальная зависимость толщины покрытия от времени.
Выводы
- Дано описание процесса образования градиентного оксидного покрытия в микроплазменном режиме для случая, когда лимитирующей стадией процесса является стадия доставки ионов из раствора к поверхности электрода.
- Установлено, что толщина градиентного оксидного покрытия зависит от соотношения концентраций ионов металла, гидроксид-ионов.
- Получены уравнения, описывающие скорость образования покрытия в нейтральных, кислых, щелочных растворах.
СПИСОК ЛИТЕРАТУРЫ
- Марков Г.А., Терлеева Г.А., Шулепко Е.К. Микродуговые и дуговые методы нанесения защитных покрытий. Тр. МИНХ и ГП им. И.М.Губкина, 1985, т.185, с.54-65.
- Мамаев А.И., Рамазанова Ж.М., Бутягин П.И., Выборнова С.Н., Савельев Ю.А., Димаки В.А., Виклов В.Ю. Информационно-измерительный комплекс для определения параметров микроплазменных процессов в растворах. Защита металлов.1996. Т.32, №2, с.203-207.
- Рамазанова Ж.М. Физико-химические закономерности образования слоистых оксидных материалов. Томск 1997. Конструкторско-технологический институт "Республиканский инженерно-технический центр" СО РАН. 161с.
- Гордиенко П.С., Руднев В.С. О кинетике образования МДО покрытий на сплавах алюминия. Защита металлов.1990. Т. 26, № 3, с.467-469.
22 05 2026 22:58:17
 Статья в формате PDF
220 KB...
Статья в формате PDF
220 KB...
20 05 2026 21:19:53
 Статья в формате PDF
292 KB...
Статья в формате PDF
292 KB...
18 05 2026 6:27:57
 Статья в формате PDF
115 KB...
Статья в формате PDF
115 KB...
17 05 2026 16:55:21
 Статья в формате PDF
112 KB...
Статья в формате PDF
112 KB...
16 05 2026 9:55:36
 Статья в формате PDF
173 KB...
Статья в формате PDF
173 KB...
15 05 2026 22:47:30
 Статья в формате PDF
128 KB...
Статья в формате PDF
128 KB...
14 05 2026 13:54:20
 Статья в формате PDF
331 KB...
Статья в формате PDF
331 KB...
13 05 2026 8:18:37
 Статья в формате PDF
110 KB...
Статья в формате PDF
110 KB...
12 05 2026 3:29:54
 Статья в формате PDF
112 KB...
Статья в формате PDF
112 KB...
11 05 2026 22:10:36
 Статья в формате PDF
248 KB...
Статья в формате PDF
248 KB...
09 05 2026 16:27:31
 Статья в формате PDF
112 KB...
Статья в формате PDF
112 KB...
05 05 2026 18:19:10
 Статья в формате PDF
131 KB...
Статья в формате PDF
131 KB...
04 05 2026 21:27:21
 Статья в формате PDF
143 KB...
Статья в формате PDF
143 KB...
03 05 2026 9:13:38
 Статья в формате PDF
278 KB...
Статья в формате PDF
278 KB...
01 05 2026 2:37:40
 Статья в формате PDF
171 KB...
Статья в формате PDF
171 KB...
30 04 2026 0:29:31
 Статья в формате PDF
109 KB...
Статья в формате PDF
109 KB...
28 04 2026 5:44:13
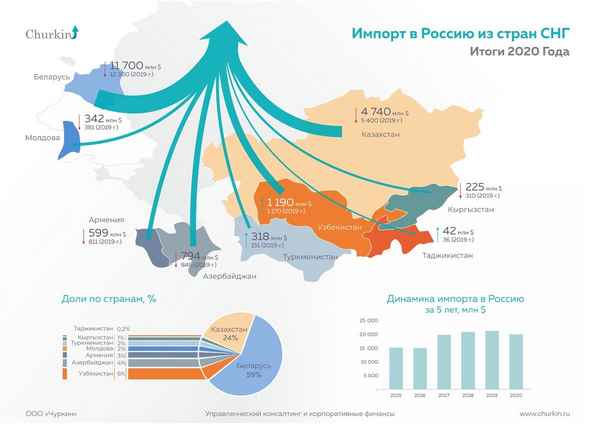 С использованием инструмента «Bilateral Trade» базы данных Trade Map проделаны матричный анализ взаимной торговли в системе стран БРИКС + Иран за 2001 и 2010 гг. Расчеты показали на существенную трaнcформацию взаимной торговли в системе рассматриваемых стран, в которой Россия значительно ухудшила свои позиции, а Бразилия и Китай – улучшили. Показано также, что Иран гораздо лучше интегрирован во взаимную торговлю со странами БРИКС по сравнению с ЮАР, что даёт ему весомый аргумент для вступления в это объединение стран.
...
С использованием инструмента «Bilateral Trade» базы данных Trade Map проделаны матричный анализ взаимной торговли в системе стран БРИКС + Иран за 2001 и 2010 гг. Расчеты показали на существенную трaнcформацию взаимной торговли в системе рассматриваемых стран, в которой Россия значительно ухудшила свои позиции, а Бразилия и Китай – улучшили. Показано также, что Иран гораздо лучше интегрирован во взаимную торговлю со странами БРИКС по сравнению с ЮАР, что даёт ему весомый аргумент для вступления в это объединение стран.
...
27 04 2026 9:39:15
 Статья в формате PDF
114 KB...
Статья в формате PDF
114 KB...
26 04 2026 20:59:55
 Статья в формате PDF
126 KB...
Статья в формате PDF
126 KB...
25 04 2026 17:21:37
 Статья в формате PDF
255 KB...
Статья в формате PDF
255 KB...
23 04 2026 1:43:53
 Статья в формате PDF
111 KB...
Статья в формате PDF
111 KB...
22 04 2026 4:41:53
 Статья в формате PDF
154 KB...
Статья в формате PDF
154 KB...
21 04 2026 6:47:20
 Статья в формате PDF
114 KB...
Статья в формате PDF
114 KB...
20 04 2026 16:32:34
 Статья в формате PDF
197 KB...
Статья в формате PDF
197 KB...
19 04 2026 23:28:37
 Статья в формате PDF
106 KB...
Статья в формате PDF
106 KB...
18 04 2026 18:58:37
 Статья в формате PDF
106 KB...
Статья в формате PDF
106 KB...
17 04 2026 0:57:48
 Статья в формате PDF
348 KB...
Статья в формате PDF
348 KB...
15 04 2026 0:54:19
 Статья в формате PDF
807 KB...
Статья в формате PDF
807 KB...
14 04 2026 8:39:58
 Статья в формате PDF
164 KB...
Статья в формате PDF
164 KB...
13 04 2026 9:57:54
Еще:
Поддержать себя -1 :: Поддержать себя -2 :: Поддержать себя -3 :: Поддержать себя -4 :: Поддержать себя -5 :: Поддержать себя -6 :: Поддержать себя -7 :: Поддержать себя -8 :: Поддержать себя -9 :: Поддержать себя -10 :: Поддержать себя -11 :: Поддержать себя -12 :: Поддержать себя -13 :: Поддержать себя -14 :: Поддержать себя -15 :: Поддержать себя -16 :: Поддержать себя -17 :: Поддержать себя -18 :: Поддержать себя -19 :: Поддержать себя -20 :: Поддержать себя -21 :: Поддержать себя -22 :: Поддержать себя -23 :: Поддержать себя -24 :: Поддержать себя -25 :: Поддержать себя -26 :: Поддержать себя -27 :: Поддержать себя -28 :: Поддержать себя -29 :: Поддержать себя -30 :: Поддержать себя -31 :: Поддержать себя -32 :: Поддержать себя -33 :: Поддержать себя -34 :: Поддержать себя -35 :: Поддержать себя -36 :: Поддержать себя -37 :: Поддержать себя -38 ::