СТРУКТУРНЫЙ МЕХАНИЗМ ФАЗОВОГО ПЕРЕХОДА Fd3m → P213 В ШПИНЕЛИ LiZn0,5Mn1,5O4
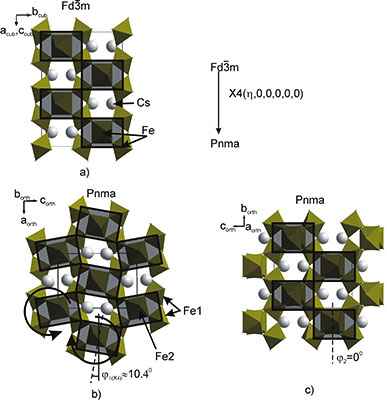
В результате фазовых превращений происходит расслоение правильных систем точек (ПСТ), которые занимают атомы лития, цинка, марганца и кислорода в исходной фазе. Из всех возможных структурных механизмов образования низкосимметричной P213-модификации, связанных с различными критическими представлениями группы Fd3m, механизм образования исследуемой низкосимметричной фазы по представлению k10(t3) + k11(t4) оказывается самым сложным и включает:
- бинарные упорядочения катионов типа 1:1 в тетраэдрических узлах 8(а) и типа 1:3 в октаэдрических позициях 16(d) шпинели;
- четверное упорядочение анионов типа 1:1:3:3 в структуре исходной фазы;
- смещения всех типов атомов.
Отметим также, что структурный механизм образования исследуемой фазы значительно сложнее, чем предполагалось ранее [1]: он не сводится только к упорядочению лития, цинка и марганца.
С помощью найденных скалярных и векторных базисных функций критического приводимого представления построена модель структуры низкосимметричной фазы (рис. 1-2).
Рис. 1. Тетраэдры и гексаэдры в структуре упорядоченной фазы
Рис. 2. Ближайшее окружение атомов в структуре P213- фазы: а - окружение Li(1); б - окружение Zn; в - окружение Mn; г - окружение Li(2); д - окружение O(1); е - окружение O(2); ж - окружение O(3); з - окружение O(4)
В низкосимметричной P213-фазе должны произойти все смещения атомов, которые совместимы с ее симметрией, задаваемой только критическими смещениями. Вблизи точки фазового перехода второго рода некритические смещения малы по сравнению с критическими. Однако по мере удаления от точки фазового перехода некритические и критические смещения могут сравняться по порядку величины и должны учитываться при расшифровке кристаллической структуры. Более того, в тех случаях, когда критическими являются смещения легких атомов, трудно определяемые рентгеновскими методами, о них можно судить по набору некритических смещений атомов, обладающих большей рассеивающей способностью.
Сравнительным анализом расчетных и экспериментальных координат атомов для упорядоченной кубической фазы литий-цинк марганцевой шпинели (медленно охлажденной от 700°С до комнатной [1]) определены интегральные (критические и некритические) величины смещений ионов из равновесных положений в неупорядоченной кубической ячейке шпинели. Величины смещений оказались равными для ионов Li(1) (a ≈ -0,008 Å), для ионов Zn (b ≈ -0,029 Å), для ионов Li(2) (c ≈ -0,016 Å), Mn (d ≈ -0,053 Å, e ≈ 0,068 Å, f ≈ -0,573 Å) и для ионов кислорода O(1) (k ≈ -0,220 Å, l ≈ 0,056 Å, m ≈ -0,152 Å), O(2) (n ≈ -0,103 Å, p ≈ -0,103 Å, r ≈ 0,194 Å), O(3) (g ≈ -0,061 Å), O(4) (h ≈ -0,116 Å). Из-за недостатка экспериментальных данных выделить некритические смещения не возможно. Значительные по величине смещения кислорода и марганца приводят к значительной деформации гексаэдров в структуре неупорядоченной шпинели.
В P213-фазе «бывшие» тетраэдрические катионы лития и цинка находятся в моновариантной позиции 4(а) с локальной симметрией 3(C3). Их ближайшее окружение различно: вокруг Li(1) расположены три кислорода О(2) и один О(4) (рис. 2, а), а вокруг Zn - три кислорода О(1) и один О(3) (рис. 2, б). Ось третьего порядка проходит соответственно вдоль связей Li(1)-О(4) и Zn-О(3). Марганец находится в трехвариантной позиции 12(в) в центре искаженного октаэдра, его локальная симметрия 1(C1). Вокруг атома Mn расположены два атома кислорода О(l), два атома кислорода О(2), один атом кислород О(3) и один атом кислород О(4) (рис. 2, в). Катионы Li(2) находятся в центре искаженного октаэдра в моновариантной позиции 4(а) с локальной симметрией 3(C3). Ближайшим окружением Li(2) являются три атома кислорода О(1) и три атома кислорода О(2) (рис. 2, г). Анионы кислорода в упорядоченной фазе разбились на две группы, в каждой из которых имеется два разных типа ближайшего окружения. Атомы кислорода О(1) и О(2) занимают тривариантные двенадцатикратные позиции 12(в) с локальной симметрией 1(C1), а атомы кислорода О(3) и О(4) занимают моновариантные четырехкратные позиции 4(а) с локальной симметрией 3(C3). Атом кислорода О(1) окружен двумя атомами марганца, одним атомом цинка и одним атомом Li(1), атом кислорода О(2) окружен двумя атомами марганца, одним атомом Li(2) и одним атомом Li(1), атом кислорода О(3) окружен тремя атомами марганца и одним атомом цинка, атом кислорода О(4) окружен тремя атомами марганца и одним атомом Li(1). Ближайшее окружение каждого из четырех типов атомов кислорода показано на рис. 2, д-з).
Таким образом, расчетная структурная формула LiZn0,5Mn1,5O4 в P213-фазе имеет вид: (Li(1)4(а)0,5Zn4(а)0,5)[Li4(а)0,5Mn12(b)1,5]O12(b)O12(b)O4(а)O4(а) и полностью согласуется с нейтронографическими и рентгеноструктурными экспериментальными данными [1].
Список литературы
1. Lee Y.J., Park S.H., Eng C., Parise J.B., Grey C.P. Cation Ordering and Electrochemical Properties of the Cathode Materials LiZnxMn2-xO4, 0 < x < 0,5: A 6Li Magic-Angle Spinning NMR Spectroscopy and Diffraction Study // Chem. Mater. - 2002. - Vol. 14. - P. 194-205.
 Статья в формате PDF
139 KB...
Статья в формате PDF
139 KB...
23 05 2026 10:46:22
 Статья в формате PDF
3943 KB...
Статья в формате PDF
3943 KB...
21 05 2026 23:23:35
 Статья в формате PDF
106 KB...
Статья в формате PDF
106 KB...
20 05 2026 15:59:16
 Эффективность фотопреобразования света в электрический ток ограничено рекомбинационными, тепловыми и другими потерями энергии в структурах солнечных элементов (СЭ). Уравнения, описывающие потери, уточнены с учетом рассредоточения омических потерь в лицевом слое (ЛС). Впервые проведена оценка тепловых потерь, обусловленных эффектом Пельтье, в контактах электрической цепи СЭ.
...
Эффективность фотопреобразования света в электрический ток ограничено рекомбинационными, тепловыми и другими потерями энергии в структурах солнечных элементов (СЭ). Уравнения, описывающие потери, уточнены с учетом рассредоточения омических потерь в лицевом слое (ЛС). Впервые проведена оценка тепловых потерь, обусловленных эффектом Пельтье, в контактах электрической цепи СЭ.
...
19 05 2026 10:11:50
 Статья в формате PDF
120 KB...
Статья в формате PDF
120 KB...
18 05 2026 9:22:58
 Статья в формате PDF
137 KB...
Статья в формате PDF
137 KB...
17 05 2026 21:15:34
 Статья в формате PDF
251 KB...
Статья в формате PDF
251 KB...
16 05 2026 1:25:19
 Статья в формате PDF
119 KB...
Статья в формате PDF
119 KB...
15 05 2026 16:54:19
 Статья в формате PDF
125 KB...
Статья в формате PDF
125 KB...
14 05 2026 22:11:13
 Статья в формате PDF
147 KB...
Статья в формате PDF
147 KB...
13 05 2026 13:14:46
 Статья в формате PDF
131 KB...
Статья в формате PDF
131 KB...
10 05 2026 8:54:54
 Статья в формате PDF
267 KB...
Статья в формате PDF
267 KB...
09 05 2026 20:20:37
 Статья в формате PDF
137 KB...
Статья в формате PDF
137 KB...
08 05 2026 5:35:17
 Бесплодие в бpaке – это не только физическое, это еще всегда психологическое и социальное нeблагополучие. В последние годы интерес к проблеме психологических факторов при бесплодии возрос. Влияние психологического состояния, обусловленного бесплодием, на результат лечения признается пpaктически всеми исследователями. Реакция на бесплодие независимо от того женское оно или мужское, сильнее выражено у женщин. Возраст и длительность бpaка не влияют на остроту стресса. Наиболее сильное чувство депрессии у женщин выражено на 2-3 год после выявления бесплодия, а после 3-4 лет начинается адаптация к бесплодию. Отмечено, что женщинам с идиопатическим бесплодием присущ больший оптимизм, в отличие от пациенток, бесплодие которых было обусловлено заболеванием, требующим хирургического лечения. В последние годы разработаны различные методики психологической коррекции и лечения психических расстройств при бесплодии.
...
Бесплодие в бpaке – это не только физическое, это еще всегда психологическое и социальное нeблагополучие. В последние годы интерес к проблеме психологических факторов при бесплодии возрос. Влияние психологического состояния, обусловленного бесплодием, на результат лечения признается пpaктически всеми исследователями. Реакция на бесплодие независимо от того женское оно или мужское, сильнее выражено у женщин. Возраст и длительность бpaка не влияют на остроту стресса. Наиболее сильное чувство депрессии у женщин выражено на 2-3 год после выявления бесплодия, а после 3-4 лет начинается адаптация к бесплодию. Отмечено, что женщинам с идиопатическим бесплодием присущ больший оптимизм, в отличие от пациенток, бесплодие которых было обусловлено заболеванием, требующим хирургического лечения. В последние годы разработаны различные методики психологической коррекции и лечения психических расстройств при бесплодии.
...
07 05 2026 22:34:51
06 05 2026 2:34:35
 Статья в формате PDF
100 KB...
Статья в формате PDF
100 KB...
05 05 2026 23:45:59
04 05 2026 1:33:46
 Статья в формате PDF
158 KB...
Статья в формате PDF
158 KB...
03 05 2026 8:10:29
02 05 2026 1:34:11
 Статья в формате PDF
120 KB...
Статья в формате PDF
120 KB...
01 05 2026 3:35:48
 Статья в формате PDF
107 KB...
Статья в формате PDF
107 KB...
30 04 2026 19:22:41
 Статья в формате PDF
104 KB...
Статья в формате PDF
104 KB...
29 04 2026 10:37:54
28 04 2026 10:45:37
 Статья в формате PDF
181 KB...
Статья в формате PDF
181 KB...
27 04 2026 0:22:59
 Статья в формате PDF
313 KB...
Статья в формате PDF
313 KB...
26 04 2026 12:15:39
25 04 2026 19:26:28
23 04 2026 18:39:25
 Статья в формате PDF
103 KB...
Статья в формате PDF
103 KB...
22 04 2026 15:59:41
Статья в формате PDF 266 KB...
21 04 2026 14:51:25
 Статья в формате PDF
102 KB...
Статья в формате PDF
102 KB...
20 04 2026 10:16:46
 Статья в формате PDF
134 KB...
Статья в формате PDF
134 KB...
19 04 2026 14:39:26
 Дана оценка современным физико-химическим методам исследования для контроля, сертификации и гигиенической оценке безопасности нономатариалов. Разработаны методики определения ряда тяжелых металлов в биологических средах, которые утверждены МЗ РФ и Роспотребнадзором РФ и могут быть использованы для оценки безопасности наноматериалов.
...
Дана оценка современным физико-химическим методам исследования для контроля, сертификации и гигиенической оценке безопасности нономатариалов. Разработаны методики определения ряда тяжелых металлов в биологических средах, которые утверждены МЗ РФ и Роспотребнадзором РФ и могут быть использованы для оценки безопасности наноматериалов.
...
18 04 2026 18:28:52
 Статья в формате PDF
297 KB...
Статья в формате PDF
297 KB...
17 04 2026 22:54:43
 Статья в формате PDF
300 KB...
Статья в формате PDF
300 KB...
16 04 2026 10:48:25
15 04 2026 1:13:51
 Статья в формате PDF
277 KB...
Статья в формате PDF
277 KB...
14 04 2026 9:22:46
Еще:
Поддержать себя -1 :: Поддержать себя -2 :: Поддержать себя -3 :: Поддержать себя -4 :: Поддержать себя -5 :: Поддержать себя -6 :: Поддержать себя -7 :: Поддержать себя -8 :: Поддержать себя -9 :: Поддержать себя -10 :: Поддержать себя -11 :: Поддержать себя -12 :: Поддержать себя -13 :: Поддержать себя -14 :: Поддержать себя -15 :: Поддержать себя -16 :: Поддержать себя -17 :: Поддержать себя -18 :: Поддержать себя -19 :: Поддержать себя -20 :: Поддержать себя -21 :: Поддержать себя -22 :: Поддержать себя -23 :: Поддержать себя -24 :: Поддержать себя -25 :: Поддержать себя -26 :: Поддержать себя -27 :: Поддержать себя -28 :: Поддержать себя -29 :: Поддержать себя -30 :: Поддержать себя -31 :: Поддержать себя -32 :: Поддержать себя -33 :: Поддержать себя -34 :: Поддержать себя -35 :: Поддержать себя -36 :: Поддержать себя -37 :: Поддержать себя -38 ::