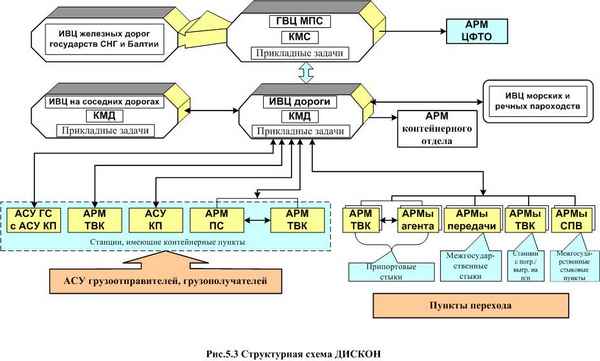
КОМПЬЮТЕРНЫЙ АНАЛИЗ ОСОБЕННОСТЕЙ ВТОРИЧНЫХ СТРУКТУР ГЛЮКОАМИЛАЗ ИЗ ASPERGILLUS AWAMORI И SACCHAROMYCOPSIS FIBULIGERA

Использование метода компьютерного моделирования позволяет не только уточнить информацию о количестве и протяженности элементов вторичной структуры белковой молекулы, но и выявить их прострaнcтвенную локализацию.
Из данных литературы следует, что в глобулярных белках, трехмерные структуры которых определены методом РСА, обычно около 60 % остатков аминокислот участвуют в формировании вторичной структуры [1-6]. Показано, что содержание α-спиралей в среднем составляет 35 %, β-слоев - 15 %, реверсивных поворотов - 20-25 %. Так как α-спираль является наиболее часто встречающимся в белках типом вторичной структуры, можно сделать предположение о ее высокой конформационной стабильности. С этим хорошо согласуется информация о расположении α-спирали в центре разрешенной области на карте Рамачандрана, а также тот факт, что диполи ее водородных связей имеют линейное расположение, отвечающее минимуму энергии. Кроме того, радиус спирали благоприятствует дисперсионному притяжению между остатками, расположенными по разные стороны от оси спирали.
Особенностью β-структуры является направление цепей. Складчатые листы с обоими направлениями цепей встречаются часто, хотя структуры, состоящие из параллельных или антипараллельных слоев, более предпочтительны.
На основе данных литературы можно заключить, что реверсивные повороты сконцентрированы на поверхности белковой глобулы, в связи с чем содержат преимущественно гидрофильные остатки [1-6]. Предполагается, что в процессе свертывания полипептидной цепи повороты играют пассивную роль, образуя участки наименьшего сопротивления невалентным силам, стремящимся изогнуть цепь. Подтверждением служит большое разнообразие наблюдаемых поворотов, ни один из которых не имеет стабильной конформации.
Содержание элементов вторичной структуры в молекулах глюкоамилаз из Aspergillus awamori и Saccharomycopsis fibuligera
|
Конформация |
Глюкоамилаза из Aspergillus awamori |
Глюкоамилаза из Saccharomycopsis fibuligera |
||
|
Номера остатков в составе структуры |
Содержание |
Номера остатков в составе структуры |
Содержание |
|
|
α-спирали |
1: 1...20 2: 54...68 3: 72...89 4: 126...144 5: 148...168 6: 186...205 7: 211... 227 8: 245...254 9: 272...285 10: 318...338 11: 345...354 12: 368...391 13: 416...429 |
27,1 |
1: 18...35 2: 69...84 3: 89...107 4: 146...163 5: 182...200 6: 218...237 7: 240...258 8: 290...298 9: 314...330 10: 364...383 11: 393...400 12: 424...447 13: 472...489 |
24,5 |
|
β-структура |
1: 21...23 2: 49...53 3: 107...109 4: 114...116 5: 173...175 6: 181...183 7: 235...237 8: 339...344 9: 360...363 10: 398...403 11: 407...415 |
22,9 |
1: 36...39 2: 50...55 3: 63...68 4: 126...129 5: 205...208 6: 210...217 7: 264...277 8: 350...357 9: 360...363 10: 385...391 11: 415...421 12: 454...459 13: 464...470 |
24,5 |
|
β-изгибы |
1: 20...21 2: 53...54 3: 338...339 4: 344...345 5: 415...416 |
10,4 |
1: 35...36 2: 68...69 3: 217...218 4: 363...364 |
7,6 |
|
Неупорядоченные участки |
1: 23...49 2: 68...72 3: 89...107 4: 109...114 5: 116...126 6: 144...148 7: 168...173 8: 175...181 9: 183...186 10:205...211 11: 227...235 12: 237...245 13: 254...272 14: 285...318 15: 354...360 16: 363...368 17: 391...398 18: 403...407 19: 429...471 |
39,6 |
1: 1...18 2: 39...50 3: 55...63 4: 84...89 5: 107...126 6: 129...146 7: 163...182 8: 200...205 9: 208...210 10:237...240 11: 258...264 12: 277...290 13: 298...314 14: 330...350 15: 357...360 16: 383...385 17: 391...393 18: 400...415 19: 421...424 20: 447...454 21: 459...464 22: 470...472 23: 489...492 |
43,4 |
На основе данных РСА с помощью программы MolScript [8] нами были построены трехмерные изображения α-спиралей, β-структур, неупорядоченных участков глюкоамилаз различного происхождения. Модели элементов вторичной структуры фермента из плесневого микромицета были созданы на основе результатов РСА A. Aleshin et. al. для глюкоамилазы-II из Aspergillus awamori X100, представляющей собой комплекс каталитического домена и N-терминального участка О-гликозилированного сайта глюкоамилазы-I [7]. Для построения трехмерного изображения молекулы глюкоамилазы дрожжевого происхождения мы использовали данные РСА A. Solovicova et. al. для энзима из Saccharomycopsis fibuligera [9]. Результаты РСА для обоих ферментов получены из Protein Data Bank, Brookhaven National Laboratory.
Анализ топологии и соотношения различных типов вторичной структуры показал, что для фрагмента субъединицы молекулы глюкоамилазы из Aspergillus awamori хаpaктерна плотная упаковка ядра в виде 13 α-спиралей, 11 β-слоев и 19 неупорядоченных участков. Расположение α-спиральных участков в структуре фермента обозначено цифрами 1-13 в порядке очередности их локализации в макромолекуле белка. Аналогичным образом представлены β-слои, β-изгибы и неупорядоченные участки (таблица).
Установлено, что α-спирали и β-слои не имеют четко выраженной тенденции располагаться в каких-то определенных местах третичной структуры (например, внутри или на поверхности глобулы, в области N- или С-конца и т.д.). Обнаружено, что среди элементов вторичной структуры отсутствуют полипролиновые спирали, π-спирали, и, очевидно, 310-спирали. Наличие пяти β-изгибов позволяет молекуле поддерживать компактность, так как с их помощью полипептидная цепь в β-слое может поворачивать назад, и поэтому такая структура менее склонна выходить за пределы глобулы.
Таким образом, на основании полученных данных можно заключить, что вторичная структура глюкоамилазы из Aspergillus awamori является упорядоченной.
Сравнение хаpaктеров свертывания полипептидных цепей в прострaнcтве позволяет устанавливать родственные связи между белками, выделенными из различных продуцентов. Поэтому аналогичный анализ особенностей вторичной структуры был осуществлен для глюкоамилазы из Saccharomycopsis fibuligera. Показано, что полипептидная цепь образует 13 α-спиралей, 13 β-слоев, 4 β-изгиба и 23 неупорядоченных участка (таблица). Установлено, что в целом топология вторичной структуры для глюкоамилаз из Aspergillus awamori и Saccharomycopsis fibuligera очень схожа. Увеличение количества β-слоев и аморфных участков в ферменте дрожжевого происхождения объясняется, вероятно, большей протяженностью полипептидной цепи. Удлинение цепи предусматривает наличие дополнительных факторов компактизации глобулы.
Количество β-изгибов (4) является явно недостаточным для компактности молекулы, в связи с чем глобула глюкоамилазы из Saccharomycopsis fibuligera имеет больший объем по сравнению с ферментом из Aspergillus awamori. Из таблицы видно, что протяженности α-спиралей анализируемых белковых структур весьма сходны, равно как и β-слоев.
В β-структуре глюкоамилазы из Saccharomycopsis fibuligera лишь седьмой слой является, вероятно, параллельным, остальные двенадцать имеют антипараллельную направленность цепей. Из таблицы следует, что вторичная структура фермента дрожжевого происхождения обладает высокой степенью упорядоченности, равно как и энзим из Aspergillus awamori.
Таким образом, нами обнаружено, что в состав вторичной структуры молекул глюкоамилаз плесневого и дрожжевого происхождения входят все основные элементы: α-спирали, β-слои, β-изгибы и неупорядоченные фрагменты полипептидной цепи. При этом β-структура анализируемых ферментов хаpaктеризуется наличием антипараллельных цепей. Выявлено, что заниженное по сравнению со среднестатистическим содержание α-спиралей компенсируется за счет увеличения количества β-слоев. Показано, что примерно 66 % аминокислотных остатков полипептидных цепей глюкоамилаз из Aspergillus awamori и Saccharomycopsis fibuligera задействованы в образовании упорядоченных элементов вторичной структуры. Топология α-спиралей, β-структур и неупорядоченных участков в молекулах анализируемых белков свидетельствует об их эволюционной близости. Полученные нами результаты хорошо согласуются с данными литературы о прострaнcтвенной организации белковых молекул [1-6].
Список литературы
- Кантор Ч. Биофизическая химия. - М.: Мир, 1984. - Т. 1. - 336 с.
- Мурзин А.Г., Финкельштейн А.В. // Биофизика. - 1983. - Т. 28, № 5. - С. 905.
- Попов Е.М. Структурно-функциональная организация белков. - М.: Наука, 1992. - 358 с.
- Степанов В.М. Молекулярная биология. Структура и функции белков. - М.: Высш. шк., 1996. - 335 с.
- Шерман С.А. Конформационный анализ и установление прострaнcтвенной структуры белковых молекул. - Минск: Наука и техника, 1989. - 240 с.
- Шульц Г. Принципы структурной организации белков. - М.: Мир, 1982. - 360 с.
- Aleshin A.E., Hoffmann C., Firsov L.M. et.al. // J. Mol. Biol. - 1994. - Vol. 238, № 6. - P. 575.
- Kraulis P. // J. Appl. Crystallogr. - 1991. Vol. 24. - P. 946.
- Solovicova A., Christensen T., Hostinova E. et.al. // Eur. J. Biochem. - 1999. - Vol. 264, № 8. - P. 756.
 Статья в формате PDF
206 KB...
Статья в формате PDF
206 KB...
22 05 2026 0:56:15
 Статья в формате PDF
257 KB...
Статья в формате PDF
257 KB...
21 05 2026 8:17:55
 Статья в формате PDF
109 KB...
Статья в формате PDF
109 KB...
20 05 2026 4:46:40
 Статья в формате PDF
116 KB...
Статья в формате PDF
116 KB...
19 05 2026 14:30:15
 Статья в формате PDF
121 KB...
Статья в формате PDF
121 KB...
18 05 2026 19:43:36
 Статья в формате PDF
119 KB...
Статья в формате PDF
119 KB...
17 05 2026 20:21:53
 Статья в формате PDF
146 KB...
Статья в формате PDF
146 KB...
16 05 2026 19:15:34
 Статья в формате PDF
329 KB...
Статья в формате PDF
329 KB...
15 05 2026 0:44:18
 Статья в формате PDF
101 KB...
Статья в формате PDF
101 KB...
14 05 2026 18:45:52
 Статья в формате PDF
154 KB...
Статья в формате PDF
154 KB...
12 05 2026 1:44:21
 Статья в формате PDF
116 KB...
Статья в формате PDF
116 KB...
10 05 2026 20:17:12
 Статья в формате PDF
132 KB...
Статья в формате PDF
132 KB...
09 05 2026 6:12:24
 Статья в формате PDF
118 KB...
Статья в формате PDF
118 KB...
08 05 2026 8:19:32
 Химия, биология, география и астрономия являются естественными науками, а обучение химии, биологии, географии и астрономии, безусловно, является искусством. И от того, насколько педагоги владеют этим искусством, зависит то, насколько наше общество вооружено знаниями. Обучение естественным наукам - это не просто передача определенного объема знаний, но и развитие жажды серьезного труда, без которой жизнь не может быть ни достойной, ни счастливой. А для того, чтобы эта жажда появилась, необходимо, чтобы сам напиток знаний был не только полезным и поучительным, но и обязательно «вкусным», содержал какие-то «наркотические компоненты», вызывающие устойчивое привыкание к получению все новых знаний. Талантливым детям необходимы талантливые учебники и талантливые образовательные системы. Нельзя сокращать количество часов преподавания естественнонаучных дисциплин, которые способствуют лучшему усвоению гуманитарных предметов, воспитывают логику, необходимую для обучения точным дисциплинам, способствуют воспитанию гуманизма. Приводится перечень проблем, которые необходимо решать при построении образовательной системы становления естественнонаучного мировоззрения у одаренных детей.
...
Химия, биология, география и астрономия являются естественными науками, а обучение химии, биологии, географии и астрономии, безусловно, является искусством. И от того, насколько педагоги владеют этим искусством, зависит то, насколько наше общество вооружено знаниями. Обучение естественным наукам - это не просто передача определенного объема знаний, но и развитие жажды серьезного труда, без которой жизнь не может быть ни достойной, ни счастливой. А для того, чтобы эта жажда появилась, необходимо, чтобы сам напиток знаний был не только полезным и поучительным, но и обязательно «вкусным», содержал какие-то «наркотические компоненты», вызывающие устойчивое привыкание к получению все новых знаний. Талантливым детям необходимы талантливые учебники и талантливые образовательные системы. Нельзя сокращать количество часов преподавания естественнонаучных дисциплин, которые способствуют лучшему усвоению гуманитарных предметов, воспитывают логику, необходимую для обучения точным дисциплинам, способствуют воспитанию гуманизма. Приводится перечень проблем, которые необходимо решать при построении образовательной системы становления естественнонаучного мировоззрения у одаренных детей.
...
07 05 2026 5:12:53
 Статья в формате PDF
259 KB...
Статья в формате PDF
259 KB...
06 05 2026 19:44:59
 Статья в формате PDF
261 KB...
Статья в формате PDF
261 KB...
05 05 2026 22:28:59
 Проведен сравнительный анализ результатов популяционно-генетических исследований по выявлению легкодиагностируемых врожденных пороков развития и наследственных заболеваний среди населения Муганской и Ширванской зон Азербайджана. Установлена высокая частота распространения нарушений ЦНС, аномалий скелета и врожденных патологий зрения. С использованием молекулярного метода полимеразно-цепной реакции идентифицированы типы мутаций β-талассемии в обследованных зонах. Планируется проведение пренатальной диагностики талассемии.
...
Проведен сравнительный анализ результатов популяционно-генетических исследований по выявлению легкодиагностируемых врожденных пороков развития и наследственных заболеваний среди населения Муганской и Ширванской зон Азербайджана. Установлена высокая частота распространения нарушений ЦНС, аномалий скелета и врожденных патологий зрения. С использованием молекулярного метода полимеразно-цепной реакции идентифицированы типы мутаций β-талассемии в обследованных зонах. Планируется проведение пренатальной диагностики талассемии.
...
04 05 2026 2:32:12
 Статья в формате PDF
122 KB...
Статья в формате PDF
122 KB...
03 05 2026 8:45:48
 Статья в формате PDF
110 KB...
Статья в формате PDF
110 KB...
01 05 2026 0:51:36
 Статья в формате PDF
116 KB...
Статья в формате PDF
116 KB...
30 04 2026 20:45:42
 Статья в формате PDF
243 KB...
Статья в формате PDF
243 KB...
29 04 2026 0:20:53
 Статья в формате PDF
113 KB...
Статья в формате PDF
113 KB...
28 04 2026 9:38:31
 Статья в формате PDF
107 KB...
Статья в формате PDF
107 KB...
26 04 2026 2:15:47
 Статья в формате PDF
269 KB...
Статья в формате PDF
269 KB...
22 04 2026 17:50:18
 Рассмотрены корреляты как дополнительные параметры описания объектов. Рассмотрены виды коррелят. Раскрывается понятие коррелятивные показатели. Показано, как влияют корреляты на качество анализа и оценки. Для этого использовано понятие информационная модель объекта. Введено понятие коррелятивной информационной модели объекта (КИМО) Введено понятие производного коррелятивного показателя. (ПКП) Показано, что использование коррелятивного показателя позволяет создавать нелинейные экономико-математические модели. Эти нелинейные модели дают более точное описание изменения стоимости комплексов из разных объектов при существенном влиянии коньюнктурных факторов. Раскрыты основы коррелятивного подхода как инструмента описания, анализа и экономической оценки. Приведены примеры использования коррелятивного подхода. Показаны преимущества коррелятивного подхода.
...
Рассмотрены корреляты как дополнительные параметры описания объектов. Рассмотрены виды коррелят. Раскрывается понятие коррелятивные показатели. Показано, как влияют корреляты на качество анализа и оценки. Для этого использовано понятие информационная модель объекта. Введено понятие коррелятивной информационной модели объекта (КИМО) Введено понятие производного коррелятивного показателя. (ПКП) Показано, что использование коррелятивного показателя позволяет создавать нелинейные экономико-математические модели. Эти нелинейные модели дают более точное описание изменения стоимости комплексов из разных объектов при существенном влиянии коньюнктурных факторов. Раскрыты основы коррелятивного подхода как инструмента описания, анализа и экономической оценки. Приведены примеры использования коррелятивного подхода. Показаны преимущества коррелятивного подхода.
...
21 04 2026 4:13:35
20 04 2026 1:38:27
 Статья в формате PDF
108 KB...
Статья в формате PDF
108 KB...
19 04 2026 12:17:24
 Статья в формате PDF
384 KB...
Статья в формате PDF
384 KB...
18 04 2026 4:54:58
 Статья в формате PDF
240 KB...
Статья в формате PDF
240 KB...
17 04 2026 13:17:16
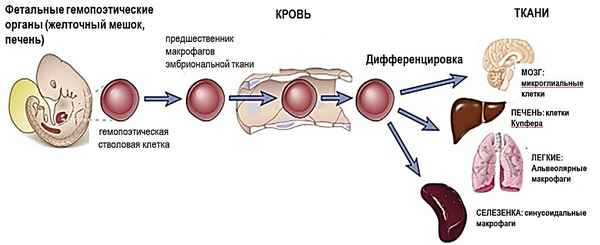 Лимфоидная закладка краниальных брыжеечных лимфатических узлов определяется у плодов белой крысы 20-21 суток в результате инфильтрации лимфоцитами их стромальных зачатков.
...
Лимфоидная закладка краниальных брыжеечных лимфатических узлов определяется у плодов белой крысы 20-21 суток в результате инфильтрации лимфоцитами их стромальных зачатков.
...
16 04 2026 1:18:26
15 04 2026 17:28:38
 В работе отражены особенности современных компьютерных и мехатронных технологий в дизайне изделий, способствующих повышению их потребительской ценности.
Раскрыта сущность и методология процесса машинного орнаментирования изделий.
...
В работе отражены особенности современных компьютерных и мехатронных технологий в дизайне изделий, способствующих повышению их потребительской ценности.
Раскрыта сущность и методология процесса машинного орнаментирования изделий.
...
14 04 2026 23:22:46
Еще:
Поддержать себя -1 :: Поддержать себя -2 :: Поддержать себя -3 :: Поддержать себя -4 :: Поддержать себя -5 :: Поддержать себя -6 :: Поддержать себя -7 :: Поддержать себя -8 :: Поддержать себя -9 :: Поддержать себя -10 :: Поддержать себя -11 :: Поддержать себя -12 :: Поддержать себя -13 :: Поддержать себя -14 :: Поддержать себя -15 :: Поддержать себя -16 :: Поддержать себя -17 :: Поддержать себя -18 :: Поддержать себя -19 :: Поддержать себя -20 :: Поддержать себя -21 :: Поддержать себя -22 :: Поддержать себя -23 :: Поддержать себя -24 :: Поддержать себя -25 :: Поддержать себя -26 :: Поддержать себя -27 :: Поддержать себя -28 :: Поддержать себя -29 :: Поддержать себя -30 :: Поддержать себя -31 :: Поддержать себя -32 :: Поддержать себя -33 :: Поддержать себя -34 :: Поддержать себя -35 :: Поддержать себя -36 :: Поддержать себя -37 :: Поддержать себя -38 ::